Nuria Rubio-Lopez , 1, 2, 3, † María Morales-Suárez-Varela , 1, 2, 3, † Yolanda Pico , 2, 4, 5, † Lorenzo Livianos-Aldana , 2, 6, 7, † e Agustín Llopis-González 1, 2, 3, *
Pubblicato su Int J Environ Res Public Health, 2016
Traduzione in italiano a cura del Dott. Claudio Ajmone per GiùleManidaiBambini.org
Testo originale in inglese, disponibile a questo link
1 Unità di Sanità Pubblica, Igiene e Salute Ambientale, Dipartimento di Medicina Preventiva e Sanità Pubblica, Scienze dell’Alimentazione, Tossicologia e Medicina Legale, Università di Valencia, Valencia 46100, Spagna; se.vu@oibur.airun (NR-L.); se.vu@selarom.m.airam (MM-S.-V.)
2Biomedical Research Center Network on Epidemiology and Public Health (CIBERESP), Madrid 28029, Spain; se.vu@ocip.adnaloy (Y.P.); se.vu@sonaivil.oznerol (L.L.-A.)
3Center for Advanced Research in Public Health (CSISP-FISABIO), Valencia 46010, Spain
4Food and Environmental Safety Research Group, Faculty of Pharmacy, University of Valencia, Valencia 46100, Spain
5Research Center on Desertification (CIDE, UV-CSIC-GV), Carretera Moncada-Náquera, Moncada 46113, Spain
6Department of Psychiatry and Clinical Psychology, La Fe University and Polytechnic Hospital, Valencia 46026, Spain
7Department of Psychiatry, University of Valencia, Valencia 46100, Spain
*Correspondence: se.vu@sipoll.nitsuga; Tel.: +34-963-544-952
†These authors contributed equally to this work.
1. Introduzione
L’infanzia è un periodo cruciale di sviluppo fisico, psicologico e sociale [1]. Sfortunatamente, questo periodo coincide frequentemente con l’inizio della malattia psichiatrica [2]. Gli attuali dati epidemiologici globali stimano che un bambino su cinque dovrebbe sviluppare una qualche forma di problema di salute mentale prima di raggiungere l’età adulta e che il 50% di tutti i problemi di salute mentale degli adulti si sviluppa durante l’infanzia e l’adolescenza [3]. Ciò evidenzia l’importanza della prevenzione e dell’intervento precoci [4].
Un’alimentazione adeguata è un noto fattore rilevante per la crescita e lo sviluppo dei bambini, non solo in termini fisiologici, ma anche per lo sviluppo ottimale delle funzioni cerebrali e cognitive [5 , 6]. Tuttavia, le prove mostrano che la qualità della dieta dei giovani è peggiorata significativamente negli ultimi decenni [7 , 8 , 9 , 10 , 11]. Un apporto inadeguato di energia o sostanze nutritive potrebbe avere un effetto dannoso sulla salute dei bambini e predisporre all’obesità infantile, alla carie dentale, scarso rendimento scolastico e bassa autostima [12 , 13 , 14 , 15].
Questo declino della qualità della dieta e un apparente aumento parallelo della prevalenza della depressione adolescenziale hanno portato a mostrare un maggiore interesse per il possibile ruolo della nutrizione nello sviluppo o nella progressione dei sintomi depressivi [7 , 16 , 17 , 18]. Gli articoli sopra citati hanno osservato che mangiare una dieta sana è significativamente associato a una migliore salute emotiva ( p <0,001), mentre mangiare una dieta malsana è significativamente associato a un maggiore disagio emotivo ( p <0,001).
Uno studio australiano [1] ha mostrato che gli adolescenti che seguono una dieta sana avevano meno probabilità di riferire depressione sintomatica, mentre coloro che mangiavano cibi “spazzatura” più elaborati avevano maggiori probabilità di riferire depressione. Jacka et al. [19] hanno riferito che la qualità della dieta è stata negativamente associata alla salute mentale degli adolescenti nel tempo. Lo stesso studio ha anche riferito che i cambiamenti nella qualità della dieta erano associati a cambiamenti nella salute mentale e che i miglioramenti nella qualità della dieta erano correlati a punteggi più alti di salute mentale al follow-up, ma non viceversa.
Uno studio sui bambini norvegesi appena pubblicato [20] hanno trovato una relazione significativa tra modelli alimentari e problemi di salute mentale nei giovani adolescenti, indipendentemente dall’attività fisica, dall’attività sedentaria e da molti altri fattori di fondo. Questo articolo ha mostrato che una qualità della dieta più scadente era associata a un declino del funzionamento psicologico. Uno studio cinese [21] ha riportato una relazione tra un modello alimentare malsano e sintomi emotivi in ragazzi di 11-16 anni.
Pochissimi studi hanno correlato l’assunzione nutrizionale ai sintomi depressivi nei bambini in Spagna, quindi sono necessari ulteriori studi per costruire conoscenze in questo campo. Data l’importanza sia della nutrizione che della salute mentale come preoccupazioni per la salute pubblica, e la scarsità di ricerche che esaminano le associazioni tra un’adeguata assunzione alimentare e problemi di salute mentale nei bambini spagnoli, il presente studio mirava a contribuire a questo campo emergente esaminando la relazione tra alimentazione assunzione e sintomi depressivi negli scolari valenciani (6-9 anni).
2. Materiali e metodi
2.1. partecipanti
ANIVA ( Antropometria y Nutrición Infantil de Valencia ; the Valencian Anthropometry and Child Nutrition) [22], uno studio descrittivo trasversale, è stato condotto su scolari di età compresa tra 6 e 9 anni che frequentavano una delle undici scuole primarie partecipanti (vedi materiali supplementari). Secondo un semplice calcolo delle dimensioni basato sui nostri dati preliminari (errore di tipo I: 0,05, potenza: 0,8), il numero stimato di soggetti era superiore a 700.
I bambini sono stati selezionati mediante campionamento casuale a grappolo nelle scuole e stratificati per sesso e tipo di scuola ( cioè , pubblico vs.privato). Quest’ultimo fattore è stato utilizzato come indicatore approssimativo dello stato socio-economico. Il campionamento è stato effettuato in due fasi: le scuole sono state selezionate da elenchi forniti dalle autorità educative regionali. Quindi, sono state selezionate le classi e gli alunni. La raccolta dei dati è avvenuta durante l’anno accademico 2013-2014. Lo studio è stato presentato oralmente al consiglio di amministrazione ( Consejo Escolar) di ciascuna scuola partecipante.
Successivamente è stata inviata una lettera ai genitori o tutori di tutti i bambini invitati a partecipare, che ha delineato gli obiettivi e le procedure dello studio e ha ottenuto la loro autorizzazione scritta. I criteri di inclusione erano: (a) bambini di età compresa tra 6 e 9 anni; (b) bambini che hanno studiato l’istruzione primaria in una delle undici scuole selezionate; e (c) i genitori o i tutori legali dovevano acconsentire alla partecipazione del loro bambino e fornire il consenso informato scritto. I criteri di esclusione erano: (a) diagnosi clinica di malattia cronica con prescrizione dietetica; (b) assenza da scuola nei giorni previsti per la misurazione del peso corporeo e dell’altezza; e (c) non completare correttamente il record nutrizionale.
Il campione iniziale comprendeva 873 bambini di entrambi i sessi, di cui il 12,8% non voleva partecipare ( N = 112). I soggetti che hanno fornito informazioni incomplete, non hanno completato correttamente la registrazione ( N = 37), o non hanno presentato dati sulle misurazioni antropometriche ( N = 14) sono stati rimossi. Il tasso di partecipazione è stato dell’81,3% e il campione finale risultante comprendeva 710 bambini.
Tutti i genitori o gli scolari dei tutori legali hanno dato il loro consenso informato per l’inclusione prima di partecipare allo studio. Il protocollo di studio è conforme alle linee guida della Dichiarazione di Helsinki ed è stato approvato dalla Secretaría Autonómica de Educación , Conserjería de Educación, Culturay Deporte della Generalitat Valenciana, Valencia, Spagna (Comitato etico 2014/29630).
2.2. Protocollo di esame e misurazioni
Genitori o tutori sono stati intervistati durante un questionario per acquisire informazioni sull’età del bambino, sesso, anamnesi, farmaci, uso di integratori vitaminici e minerali e altre caratteristiche demografiche. Allo stesso tempo, sono stati forniti dettagli su come valutare il cibo e le bevande che il loro bambino ha consumato. È stato chiesto loro di registrare le dimensioni delle porzioni stimate per ogni articolo ingerito. La stessa formazione è stata impartita alle badanti responsabili dei bambini nelle mense scolastiche. È stata fornita una guida visiva per migliorare l’accuratezza delle stime delle dimensioni delle porzioni, essenziale per ottenere dati affidabili. Ai genitori è stato chiesto di presentare etichette alimentari con ingredienti, marchi, ingredienti aggiunti e ricette per piatti fatti in casa, quando possibile. Hanno ricevuto un numero di telefono per informazioni e supporto.
2.3. Valutazione dietetica
Per svolgere l’indagine dietetica, ai genitori e ai tutori è stato chiesto di registrare tutti gli alimenti e le bevande consumati dal loro bambino in un periodo di tre giorni, incluso un giorno non lavorativo (ad es. domenica o sabato) [23 , 24 , 25] . Per calcolare l’assunzione di calorie e macro e micronutrienti di nota rilevanza per la salute pubblica, i ricercatori hanno inserito i dati dei registri alimentari in un software open source. Questo programma (DIAL ® , v2.16, Madrid, Spagna) [26], sviluppato dal Dipartimento di Nutrizione e Dietetica dell’Università Complutense di Madrid (Spagna), è stato precedentemente convalidato in Spagna per valutare le diete e gestire i dati nutrizionali. Questo software aperto include un elenco di alcuni degli alimenti arricchiti/fortificati comunemente disponibili in Spagna, ai quali possono essere aggiunti altri elementi e gli alimenti possono essere aggiunti al database. In questo modo abbiamo potuto includere la composizione nutrizionale degli alimenti confezionati prelevati dalle etichette alimentari.
2.4. Stima dell’adeguatezza/deficienza dei nutrienti
Le assunzioni dietetiche di riferimento (DRI) [27 , 28 , 29] includono i valori per le indennità dietetiche raccomandate (RDA), i requisiti medi stimati (EAR), le assunzioni adeguate (AI) e i livelli di assunzione superiori tollerabili (UL), nonché l’energia stimata Requisiti (EER) per l’energia e Intervalli accettabili di distribuzione dei macronutrienti (AMDR) per i macronutrienti.
Per ciascun nutriente, i bambini sono stati classificati come a rischio di assunzione inadeguata in base al raggiungimento o meno dei corrispondenti obiettivi nutrizionali [30] e DRI [31] proposti per la popolazione spagnola. Sono stati effettuati confronti con i DRI utilizzati negli Stati Uniti per esplorare possibili differenze. La probabilità di un’assunzione adeguata e abituale di un dato nutriente è stata calcolata come segue: z-score = (assunzione di nutrienti stimata – EAR)/DS di EAR [32].
Abbiamo usato gli EAR per i micronutrienti, quando disponibili, e abbiamo preso i valori AI per i nutrienti per i quali gli EAR non sono stati determinati. È stata inoltre calcolata e confrontata con gli AMDR la percentuale di energia fornita da proteine, lipidi e carboidrati. Utilizzando i dati raccolti sugli alimenti consumati, abbiamo effettuato valutazioni nutrizionali per i seguenti apporti: energia totale (calorie), carboidrati, lipidi, proteine, fibre, tiamina, riboflamina, niacina, acido pantotenico, vitamina B6, biotina, vitamina B12, C, D ed E; e minerali: calcio, fosforo, magnesio, ferro, zinco, iodio, selenio e fluoruro. Per ogni nutriente ritenuto dannoso (es. colesterolo) è stata applicata l’interpretazione opposta.
2.5. Misure antropometriche
Durante l’orario scolastico, l’altezza e il peso dei bambini sono stati registrati con i bambini a piedi nudi in abiti leggeri dalla stessa persona seguendo le procedure standard descritte dall’Organizzazione Mondiale della Sanità (OMS) [33]. Tutte le misurazioni antropometriche sono state ottenute in duplicato e mediate. Il peso è stato misurato con l’approssimazione di 0,05 kg utilizzando una bilancia digitale con cella di carico elettronica calibrata (OMRON BF511 ® , Tokyo, Giappone) e l’altezza (in cm) è stata misurata con uno stadiometro (Seca 213 ®, Amburgo, Germania).
Seguendo le Raccomandazioni GPC del Ministero spagnolo della salute e delle politiche sociali, abbiamo preso l’IMC come indice per calibrare lo stato nutrizionale perché è una misura facile da ottenere, è efficiente ed è stata adottata a livello internazionale come un ragionevole indicatore dell’accumulo di grasso sottocutaneo [34]. Con questi dati, abbiamo calcolato l’IMC per età (z-score) con il software WHO Anthro, v.3.2 (Ginevra, Svizzera) [35]. Sulla base della classifica percentile ottenuta, l’IMC è stato utilizzato per classificare i bambini in una delle quattro categorie [36]: sottopeso (≤5° percentile), normopeso (da >5° a <85° percentile), sovrappeso (da ≥85° a <95° percentile), o obeso (≥95° percentile).
La plica cutanea tricipitale è stata misurata alla sommità dell’arto superiore non dominante a metà tra l’acromion e l’olecrano, che era rilassato e posto parallelamente all’asse (tecnica di Durnin et al. [37]) . Le determinazioni sono state effettuate in triplicato con un calibro per plicopatie (Holtein LTD, Pembs, UK) prima di calcolare la media.
2.6. Misure di salute mentale
I sintomi depressivi sono stati valutati utilizzando il questionario del Center for Epidemiological Studies Depression Scale for Children (CES-DC) [38], un inventario della depressione auto-segnalato di 20 elementi con punteggi che vanno da 0 a 60. I punteggi più alti indicano un aumento dei sintomi depressivi. Ogni risposta a un elemento è stata valutata su una scala Likert a quattro punti da 0 a 3 e i partecipanti sono stati classificati come depressi se avevano un punteggio CES-DC di ≥15 [38]. L’affidabilità interna del CES-DC in questo studio era elevata (alfa di Cronbach = 0,86). Nessun bambino stava assumendo farmaci antidepressivi.
2.7. Analisi statistica
Le variabili continue sono espresse come medie (deviazioni standard, DS), mentre le variabili categoriali sono espresse come frequenza (percentuali, %). Il test di Kolmogorov-Smirnov è stato utilizzato per determinare la normalità della distribuzione delle variabili esaminate. Per il confronto delle medie tra i gruppi è stata utilizzata un’analisi della varianza unidirezionale con la regola di Bonferroni per correggere l’inflazione nell’errore di tipo 1 dovuto a confronti multipli post hoc . Il test Chi-quadrato è stato utilizzato per esplorare l’associazione tra variabili categoriali e il test Z a due campioni per le proporzioni per più post hoc confronti.
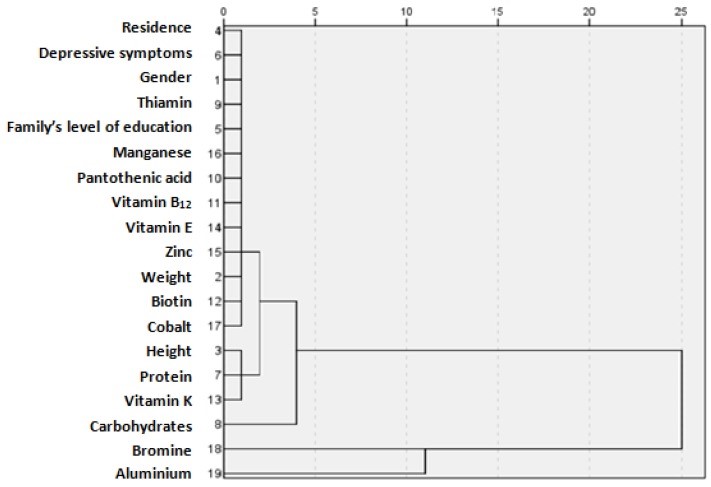
Abbiamo effettuato un confronto multivariato dei sintomi depressivi negli scolari mediante un confronto cluster analysis delle caratteristiche demografiche (residenza, sesso, livello di istruzione familiare, peso e altezza) e apporti di nutrienti (tiamina, manganese, acido pantotenico, zinco, biotina, cobalto , proteine, carboidrati, bromo, alluminio, vitamina B12, E e K), che erano significativi ( p<0,05) nelle analisi precedenti rispetto ai bambini con e senza sintomi depressivi. Un dendrogramma a grappolo produce dendrogrammi (chiamati anche alberi a grappolo) per il raggruppamento gerarchico. I dendrogrammi presentano graficamente le informazioni su cui sono raggruppate le osservazioni a vari livelli di (dis)somiglianza. A sinistra del dendrogramma, ogni osservazione è considerata il proprio cluster.
Le linee orizzontali si estendono per ogni osservazione e, a vari valori di (dis)somiglianza, queste linee sono collegate alle linee di altre osservazioni con una linea verticale. Le osservazioni continuano a combinarsi finché, a destra del dendrogramma, sono tutte raggruppate insieme. Lunghe linee orizzontali indicano una separazione più netta tra i gruppi. Le lunghe linee orizzontali a destra del dendrogramma indicano che i gruppi rappresentati da queste linee sono ben separati l’uno dall’altro. Le linee più corte indicano i gruppi che non sono così distinti. Tutti ii valori di p erano a due code e la significatività statistica è stata fissata al cut-off convenzionale di p <0,05. I dati sono stati inseriti in un foglio di calcolo Excel utilizzando una doppia immissione di dati per ridurre al minimo il rischio di errori e sono stati quindi trasferiti al software IBM SPSS versione 17.0 (SPSS Inc., Chicago, IL, USA).
3. Risultati
Tabella 1 riporta le caratteristiche demografiche del campione di studio, che comprendeva 710 scolari. Il campione comprendeva 372 ragazze (52,39%) e 338 ragazzi (47,61%). Nel 20,70% ( n = 147), gli studenti sono stati classificati come affetti da sintomi depressivi con un punteggio CES-DC ≥15. L’età media, la piega tricipitale media, l’IMC e la nazionalità erano simili nei gruppi con sintomi depressivi e con sintomi non depressivi. Tuttavia, quando sono stati analizzati sesso, altezza, peso, BMI per età, residenza e basso livello di istruzione familiare tra entrambi i gruppi, è stata osservata una differenza statisticamente significativa ( p <0,05).
Tabella 1
Caratteristiche demografiche degli scolari basate sulla classificazione dei sintomi depressivi.
| Variabili | Sintomi non depressi ( n = 563) Media ± DS o n (%) | 95% CI | Sintomi depressivi ( n = 147) Media ± DS o n (%) | 95% CI | p Valore |
| Età (anni) | 8.21 ± 1.32 | 8.10–8.32 | 8,08 ± 1,14 | 7,90–8,26 | 0.274 |
| Sesso del bambino | |||||
| Maschio | 283 (50.27) | 46.06–54.47 | 55 (37.41) | 29.69–45.81 | 0.005 |
| Femmina | 280 (49,73) | 45,53–53,94 | 92 (62.59) | 54.19–70.31 | 0.005 |
| Altezza (cm) | 131.19 ± 8.74 | 130,47–131,91 | 127,89 ± 8,99 | 126,44–129,34 | 0.001 |
| Peso (kg) | 31,85 ± 7,71 | 31.21–32.49 | 29,60 ± 8,00 | 28.31–30.89 | 0.002 |
| Piega tricipitale (mm) | 12,81 ± 4,54 | 12.43–13.19 | 12,60 ± 4,41 | 11.89-13.31 | 0,616 |
| BMI per età (punteggio z) | 1,19 ± 0,98 | 1.11-1.27 | 1,37 ± 0,97 | 1,21-1,53 | 0,047 |
| BMI | 18.31 ± 3.02 | 18.06-18.56 | 17,83 ± 3,20 | 17.31–18.35 | 0,091 |
| Sottopeso | 51 (9.06) | 6.88–11.81 | 8 (5.44) | 2,55-10,80 | 0,157 |
| normopeso | 297 (52,75) | 48.54–56.93 | 80 (54.42) | 46.02–62.58 | 0,718 |
| Sovrappeso | 114 (20.25) | 17.05–23.86 | 25 (17.01) | 11.51–24.27 | 0,377 |
| Obesità | 101 (17.94) | 14.91–21.42 | 34 (23.13) | 16,85–30,46 | 0,153 |
| Residenza | |||||
| Urbano | 311 (55,24) | 51.02–59.38 | 67 (45.58) | 37,41–53,98 | 0,037 |
| Rurale | 252 (44,76) | 40,61–48,98 | 80 (54.42) | 46.02–62.58 | 0,037 |
| Livello di istruzione della famiglia | |||||
| Basso | 93 (16.52) | 13.60–19.91 | 42 (28.57) | 21.58–36.70 | 0.001 |
| medio | 277 (49.20) | 45,00–53,41 | 55 (37.41) | 29.69–45.81 | 0,118 |
| alto | 193 (34.28) | 30.39–38.39 | 50 (34.01) | 26.54–42.34 | 0,951 |
| Nazionalità | |||||
| spagnolo | 445 (79.04) | 75.39–82.28 | 114 (77,55) | 69,79–83,84 | 0,694 |
| Altro | 118 (20.96) | 17.72-24.61 | 33 (22,45) | 16.16–30.21 | 0,694 |
Note: BMI: Indice di massa corporea; SD: Deviazione Standard; CI: Intervallo di confidenza; valore p <0,05: è stato considerato statisticamente significativo.
L’assunzione di macronutrienti, micronutrienti e minerali è stata confrontata tra i bambini con sintomi depressivi e non depressivi, come mostrato in Tavolo 2, insieme ai DRI (EER, EAR o AI) per i bambini. Sono state riscontrate differenze statisticamente significative tra entrambi i gruppi per l’assunzione di proteine, carboidrati, acido pantotenico, biotina, vitamina B12, vitamina E, zinco, manganese, cobalto, alluminio e bromo ( p <0,05), ed era inferiore nei bambini con depressione sintomi.
Differenze statisticamente significative sono state trovate anche per tiamina e vitamina K ( p K<0,05), ma l’assunzione era inferiore nel gruppo non depressivo. Più del 90% dei bambini di entrambi i gruppi ha riferito un’assunzione inadeguata di carboidrati, fibre e fluoro. Più del 50% ha indicato un’assunzione insufficiente di vitamine D, vitamina E, zinco e iodio. Abbiamo identificato differenze statisticamente significative tra i bambini con sintomi depressivi e sintomi non depressivi secondo i DRI per gli apporti di energia totale ( p = 0,026), vitamina C ( p < 0,001), vitamina E ( p = 0,004), magnesio ( p = 0,018), e ferro ( p = 0,013), che erano più bassi nei bambini con sintomi depressivi, mentre la fibra ( p < 0,001) era più alta negli stessi bambini.
Tavola 2
Assunzione di nutrienti e inadeguatezza dei nutrienti nei bambini con sintomi depressivi e non depressivi.
| Nutrienti | Sintomi non depressivi ( n = 563) Media ± DS | Sintomi depressivi ( n = 147) Media ± DS | valore p |
| Energia totale (kcal/giorno) | 2155,47 ± 344,45 | 2110,75 ± 340,87 | 0,160 |
| Percentuale con assunzione <EER (1900) | 29,9 | 39.2 | 0,026 |
| Proteine (g/giorno) | 85,74 ± 14,87 | 82,63 ± 12,97 | 0,021 |
| Percentuale con assunzione < EAR (10%-15% TEV) | 0.0 | 0.0 | – |
| Carboidrati (g/giorno) | 218,43 ± 41,85 | 210,68 ± 41,73 | 0,045 |
| Percentuale con assunzione < EAR (50%–60% TEV) | 94,2 | 96,4 | 0.238 |
| Lipidi (g/giorno) | 95,48 ± 21,50 | 95.49 ± 18.37 | 0,996 |
| Percentuale con assunzione < EAR (30%-35% TEV) | 2.0 | 2.3 | 0.238 |
| Fibra (g/giorno) | 13.78 ± 4.36 | 14.42 ± 3.97 | 0.107 |
| Percentuale con assunzione < IA (25 mg/giorno) | 98,13 | 92,3 | 0.001 |
| Tiamina (mg/giorno) | 1,37 ± 0,35 | 1,43 ± 0,19 | 0,045 |
| Percentage with intake < EAR (0.8 mg/day) | 5.78 | 6.41 | 0.904 |
| Riboflavin (mg/day) | 1.82 ± 0.50 | 1.86 ± 0.49 | 0.386 |
| Percentage with intake < EAR (1.2 mg/day) | 7.17 | 9.82 | 0.324 |
| Niacin (mg/day) | 34.04 ± 7.36 | 33.28 ± 6.64 | 0.256 |
| Percentage with intake < EAR (12 mg/day) | 0.17 | 0.00 | – |
| Pantothenic acid (mg/day) | 5.46 ± 1.05 | 5.26 ± 1.12 | 0.042 |
| Percentage with intake < AI (3 mg/day) | 0.89 | 1.36 | 0.962 |
| Vitamin B6 (mg/day) | 1.96 ± 0.63 | 2.06 ± 0.50 | 0.072 |
| Percentage with intake < EAR (1.4 mg/day) | 15.07 | 10.20 | 0.129 |
| Biotin (µg/day) | 27.23 ± 0.86 | 26.45 ± 0.37 | 0.001 |
| Percentage with intake < EAR (12) | 1.60 | 3.6 | 0.286 |
| Folic acid (µg/day) | 236.03 ± 66.503 | 227.50 ± 68.37 | 0.169 |
| Percentage with intake < EAR (200) | 35.84 | 42.16 | 0.159 |
| Vitamin B12 (µg/day) | 5.89 ± 3.36 | 5.21 ± 1.38 | 0.016 |
| Percentage with intake < EAR (1.5 µg/day) | 0.0 | 1.36 | – |
| Vitamin C (mg/day) | 105.99 ± 38.51 | 99.14 ± 35.61 | 0.052 |
| Percentage with intake < EAR (55) | 6.10 | 18.72 | 0.001 |
| Vitamin A (µg/day) | 481.90 ± 110.36 | 461.71 ± 116.56 | 0.051 |
| Percentage with intake < EAR (400 µg/day) | 8.89 | 12.44 | 0.217 |
| Vitamin D (µg/day) | 2.71 ± 3.20 | 2.98 ± 2.24 | 0.336 |
| Percentage with intake < EAR (5 µg/day) | 83.81 | 80.25 | 0.304 |
| Vitamin E (mg/day) | 8.13 ± 3.55 | 7.34 ± 3.03 | 0.014 |
| Percentage with intake < EAR (8 mg/day) | 52.80 | 66.18 | 0.004 |
| Vitamin K (µg/day) | 114.61 ± 51.22 | 129.10 ± 51.79 | 0.002 |
| Percentage with intake < EAR (55 µg/day) | 0.0 | 0.0 | – |
| Calcium (mg/day) | 940.99 ± 235.88 | 934.50 ± 296.60 | 0.779 |
| Percentage with intake < EAR (800 mg/day) | 28.83 | 35.72 | 0.087 |
| Phosphorus (mg/day) | 1396.76 ± 251.51 | 1400.29 ± 333.56 | 0.888 |
| Percentage with intake < EAR (700 mg/day) | 0.53 | 1.36 | 0.607 |
| Magnesium (mg/day) | 287.36 ± 52.43 | 279.75 ± 74.97 | 0.156 |
| Percentage with intake < IA (180 mg/day) | 5.06 | 10.23 | 0.018 |
| Iron (mg/day) | 13.86 ± 4.19 | 13.28 ± 3.54 | 0.124 |
| Percentuale con assunzione < EAR (9 mg/giorno) | 9.15 | 16.21 | 0,013 |
| Zinco (mg/giorno) | 9,60 ± 1,84 | 9,09 ± 1,76 | 0.003 |
| Percentuale con assunzione < EAR (10 mg/giorno) | 72.41 | 77.38 | 0.213 |
| Iodio (µg/giorno) | 95.74 ± 28.52 | 91,07 ± 28,89 | 0,078 |
| Percentuale con assunzione < EAR (90 µg/giorno) | 48.73 | 57.11 | 0,067 |
| Fluoro (µg/giorno) | 211,93 ± 60,00 | 205,11 ± 78,84 | 0.253 |
| Percentuale con assunzione < IA (1000 µg/giorno) | 93.61 | 96.56 | 0,166 |
| Selenio (µg/giorno) | 107,53 ± 28,22 | 105,40 ± 26,43 | 0,409 |
| Percentuale con assunzione < EAR (30 µg/giorno) | 0.0 | 0.0 | – |
| Manganese (mg giorno) | 3.09 ± 2.38 | 2,63 ± 1,26 | 0,024 |
| Percentuale con assunzione < IA (2 mg/giorno) | 6.83 | 9.84 | 0.250 |
| Cobalto (µg/giorno) * | 20.22 ± 36.10 | 11,88 ± 21,09 | 0.007 |
| Alluminio (µg/giorno) * | 497,84 ± 208,57 | 453.03 ± 201.31 | 0.020 |
| Bromo (µg/giorno) * | 432,08 ± 338,94 | 498,34 ± 445,74 | 0,049 |
Note: EER: fabbisogno energetico stimato; EAR: Requisiti medi stimati; AI: Assunzioni adeguate; SD: Deviazione Standard; CI: Intervallo di confidenza; valore p <0,05: è stato considerato statisticamente significativo; * i DRI di cobalto, alluminio e bromo non sono stati determinati.
Come risultato dell’analisi multivariata del cluster gerarchico, in cui residenza, sesso, tiamina, livello di istruzione familiare, manganese, acido pantotenico, vitamina B12, vitamina E, zinco, peso, biotina, cobalto, altezza, proteine, vitamina K, carboidrati , bromo e alluminio sono stati valutati, abbiamo ottenuto due cluster: il primo era più associato ai sintomi depressivi dei bambini, insieme alle loro caratteristiche personali (sesso, peso, altezza), ambiente (residenza urbana/rurale, livello di istruzione dei genitori), e nutrienti spiccavano (tiamina, manganese, acido pantotenico, vitamina B 12, vitamina E, zinco, biotina, cobalto, proteine, vitamina K). Infine, i carboidrati sono stati raggruppati con i precedenti nutrienti. Il secondo cluster non era direttamente correlato ai sintomi depressivi dei bambini e l’assunzione di bromo e alluminio è risultata meno correlata con i sintomi depressivi rispetto alle altre variabili dello studio (Figura 1).
4. Discussione
La depressione infantile ha un impatto sociale e sanitario sulla società, quindi la sua diagnosi precoce è prioritaria [39]. In questo studio trasversale sugli scolari spagnoli, abbiamo identificato che il 20,7% del campione presentava sintomi depressivi. Questo è il primo studio sugli scolari spagnoli a valutare tale prevalenza in questa fascia di età (6-9 anni), che è un risultato simile a quello di Steinhausen et al. [40], che ha ottenuto un risultato del 23,6%.
Altri studi hanno indicato tassi di prevalenza che variavano dallo 0,3% al 6,4% [41 , 42]. Nel nostro studio, i bambini con sintomi di depressione provenivano da famiglie con livelli di istruzione più bassi ( p <0,001), residenza rurale ( p= 0,037) e sesso femminile ( p = 0,005), rispetto a quelli senza sintomi di depressione. Alcuni autori hanno riportato che la depressione nell’infanzia è più frequente nelle ragazze che nei ragazzi [43 , 44], sebbene questa differenza non sia stata sempre osservata [41 , 45]. La maggior parte della letteratura dimostra un’elevata prevalenza di depressione nei bambini sovrappeso e obesi [46 , 47].
Abbiamo trovato una simile prevalenza di sovrappeso e obesità tra entrambi i gruppi [48 , 49]. Non è chiaro se la depressione porti all’obesità come risposta al cambiamento dell’appetito, o se l’obesità contribuisca ai disturbi depressivi [50]. I nostri risultati hanno suggerito che i bambini di età compresa tra 6 e 9 anni hanno mostrato scarsa conformità con gli obiettivi nutrizionali fissati dai DRI per la popolazione spagnola [30 , 31] (più del 25% ha mostrato un apporto inadeguato di carboidrati, fibre, acido folico, vitamina D, vitamina E, calcio, zinco, iodio e fluoro, indipendentemente dal gruppo di appartenenza).
Vale la pena sottolineare che le stime di assunzione al di sotto delle raccomandazioni non hanno indicato carenze nutrizionali poiché le assunzioni raccomandate hanno superato di gran lunga il fabbisogno medio. Tuttavia, sono utili per indicare potenziali carenze nei bambini con sintomi depressivi, che aumenteranno quanto più grandi diventano le differenze tra quelle calcolate in base alle assunzioni reali e raccomandate (DRI). I veri stati di carenza dovrebbero essere diagnosticati con altri mezzi, in particolare analisi biochimiche [51 , 52 , 53].
Diversi studi [54 , 55 , 56] hanno stabilito che una dieta di scarsa qualità, priva di alimenti ricchi di nutrienti, può portare a carenze nutrizionali, che sono state associate a problemi di salute mentale. L’alimentazione gioca forse un ruolo decisivo nell’insorgenza della depressione, nella sua gravità e durata. Numerosi modelli alimentari che precedono la depressione sono stati identificati nella depressione, come voler mangiare molti cibi dolci, saltare i pasti o non avere appetito [57].
Nel presente studio, i bambini con sintomi depressivi hanno riportato una minore assunzione di carboidrati rispetto al gruppo con sintomi non depressivi. I carboidrati svolgono un ruolo importante nella struttura e nel funzionamento dell’organismo, influenzano l’umore e il comportamento [57] e sono la più importante fonte di energia [58]. L’assunzione di carboidrati influisce sul sistema nervoso perché forniscono glucosio ed energia e influenzano la sintesi dei neurotrasmettitori nel cervello e l’attivazione del sistema nervoso simpatico.
Di conseguenza, l’ingestione di carboidrati ha un effetto positivo su diversi comportamenti umani, tra cui appetito, sonno, attività, umore, cognizione e prestazioni fisiche [59], che può avere un’influenza anche quando i sintomi depressivi sono assenti. Mangiare pasti ricchi di carboidrati innesca il rilascio di insulina. L’insulina aiuta la glicemia a entrare nelle cellule, dove può essere utilizzata per produrre energia e per attivare contemporaneamente l’ingresso del triptofano nel cervello. Nel cervello, il triptofano influenza i livelli dei neurotrasmettitori [57] perché è il precursore della serotonina cerebrale. Gli individui con livelli più bassi di serotonina cerebrale sono considerati vulnerabili alla depressione [56]. A differenza di altri studi [56 , 60] l’assunzione di fibre nel nostro studio era inferiore nei bambini senza sintomi depressivi.
È stato scoperto che le vitamine del gruppo B sono implicate nello sviluppo della depressione attraverso il metabolismo dei neurotrasmettitori [61]. I nostri dati hanno indicato che gli scolari con sintomi depressivi per lo più avevano un apporto di vitamine inferiore rispetto a quelli senza sintomi depressivi; Il 42,16% di quelli con sintomi depressivi ha mostrato un’assunzione inadeguata di acido folico secondo i DRI [57]. L’assunzione di acido folico è molto importante perché il metabolita attivo del folato è coinvolto nella metilazione dell’omocisteina e anche nella produzione di metionina, necessaria per diverse importanti vie di trasduzione del segnale che coinvolgono i neurotrasmettitori monoaminici. Quindi la carenza di folati potrebbe aumentare i livelli di omocisteina, che sono stati associati alla depressione [61 , 62]. Un basso livello di folati e vitamina B12 è stato riscontrato in studi condotti con pazienti depressi e un’associazione tra depressione e bassi livelli di queste due vitamine è stata trovata in studi condotti con la popolazione generale [63].
Secondo studi precedenti [56 , 64], gli antiossidanti sono importanti per prevenire e curare la depressione perché aiutano a ridurre lo stress ossidativo e il danno cellulare causato dai radicali liberi [65]. Ciò si verifica con la vitamina C, che si ritiene sia efficace nella depressione dato il suo ruolo nei processi ossidativi [50 , 66]. Abbiamo scoperto che l’assunzione di vitamina C era inferiore negli scolari con sintomi depressivi e abbiamo identificato una differenza statisticamente significativa in base ai DRI ( p <0,001). Più del 50% di tutti i nostri scolari presentava assunzioni di vitamina D ed E al di sotto dei DRI [56].
Ataie-Jafaei et al. [64] e Llewellyn et al. [67] hanno riportato associazioni significative tra carenza di vitamina D e disagio psichiatrico auto-riferito, come la depressione. Non abbiamo trovato associazioni significative tra loro, ma abbiamo identificato una differenza statisticamente significativa solo per la vitamina E sia nei gruppi con sintomi depressivi che con sintomi non depressivi secondo i DRI ( p = 0.004), sebbene l’assunzione di questa vitamina fosse inferiore rispetto al gruppo di sintomi non depressivi ( p = 0,014). Bassi livelli di vitamina E indicano minori difese antiossidanti contro la perossidazione lipidica, che aumentano nella depressione [68].
Oltre agli antiossidanti, alcuni minerali (magnesio, calcio, zinco, manganese e ferro) sono importanti per prevenire e curare la depressione [56] e sono stati inversamente associati alla prevalenza dei sintomi depressivi [69]. L’assunzione di questi nutrienti era inferiore nel gruppo con sintomi depressivi rispetto a quello con sintomi non depressivi. L’insufficienza di magnesio porta alla depressione a causa del danno neuronale, che si verifica quando i requisiti di magnesio dei neuroni non sono soddisfatti [50]. L’assunzione inadeguata di zinco, ferro e manganese nella dieta contribuisce ai sintomi depressivi [50 , 70]. Tutti contribuiscono alla funzione cerebrale [71].
Le assunzioni di calcio, iodio e fluoro erano ben al di sotto di quelle raccomandate in entrambi i gruppi, che coincidevano con altri autori [72 , 73], ma non sono state riscontrate differenze tra i gruppi. I nostri risultati hanno evidenziato le potenziali implicazioni significative per la salute pubblica di un apporto nutrizionale inadeguato sulla salute mentale degli scolari. Pertanto, la sorveglianza dell’assunzione alimentare può consentire la diagnosi precoce e la prevenzione dei deficit nutrizionali, che sono di vitale importanza per la corretta crescita e lo sviluppo mentale dei bambini.
Limiti dello studio
Questo studio non è esente da limiti di studio, il primo dei quali è la nostra piccola dimensione del campione. I dati che avevamo a disposizione erano insufficienti per stabilire una chiara relazione tra adeguatezza nutrizionale e sintomi depressivi. Sono necessari futuri studi su larga scala su questo tema. In secondo luogo, uno studio trasversale non fa distinzione tra causa ed effetto; non si può escludere la possibilità che la depressione sia influenzata anche da qualche percorso biologico o funzionale, abitudini alimentari, ecc. Sono necessarie ulteriori ricerche basate su studi longitudinali per esaminare l’associazione causale tra danno nutrizionale e sintomi depressivi. Riteniamo che il nostro studio offra una forte validità interna dato il basso tasso di abbandono ottenuto. Siamo fiduciosi che le informazioni auto-riferite utilizzate per la valutazione nutrizionale siano di buona qualità. I genitori e le scuole erano molto interessati allo studio e sono stati ampiamente formati e supportati per completare i registri alimentari.
Conclusioni
L’inadeguatezza nutrizionale svolge un ruolo importante nella salute mentale e nella cattiva alimentazione e può contribuire alla patogenesi della depressione. I nostri dati identificano che i carboidrati erano il fattore più strettamente associato ai sintomi depressivi negli scolari. Altri nutrienti, inclusi antiossidanti e minerali alimentari, hanno anche una forte plausibilità biologica nell’influenzare la normale funzione cerebrale e nel modulare l’umore. In termini demografici, gli scolari erano ad alto rischio di sintomi depressivi se il livello di istruzione della loro famiglia era più basso e la loro residenza era rurale. È anche importante sottolineare l’importanza di progettare programmi di educazione alimentare per consentire alla popolazione in generale, e agli scolari in particolare, di essere consapevoli e prepararsi ad abitudini alimentari sane. In questo modo.
Ringraziamenti
Desideriamo ringraziare tutti i bambini e i loro genitori che hanno partecipato a questo studio.
Abbreviazioni
In questo manoscritto vengono utilizzate le seguenti abbreviazioni:
| BMI | Indice di massa corporea |
| CES-D | Center for Epidemiologic Studies Depression Scale |
| DRI | Assunzioni dietetiche di riferimento |
| ANIVA | Antropometria y Nutrición Infantil de Valencia |
| RDA | Dosi dietetiche consigliate |
| ORECCHIO | Requisiti medi stimati |
| AI | Assunzioni adeguate |
| UL | Livelli di assunzione superiori tollerabili |
| EER | Fabbisogno energetico stimato |
| AMDR | Intervalli di distribuzione dei macronutrienti accettabili |
| OMS | Organizzazione mondiale della Sanità |
| SD | Deviazione standard |
Materiali supplementari
Clicca qui per il file di dati aggiuntivi. (148K, pdf)
Contributi dell’autore
Nuria Rubio-Lopez, Agustin Llopis-González e Maria Morales-Suarez-Varela hanno avuto l’idea originale per lo studio, mentre tutti i coautori hanno realizzato il design. Yolanda Pico e Lorenzo Livianos-Aldana erano responsabili del reclutamento e del follow-up dei partecipanti allo studio. Yolanda Pico, Lorenzo Livianos-Aldana e Maria Morales-Suarez-Varela erano responsabili della pulizia dei dati e Agustin Llopis-Gonzalez e Nuria Rubio Lopez hanno effettuato le analisi. Nuria Rubio-Lopez, Agustin Llopis-González, Maria Morales-Suarez-Varela, Yolanda Pico e Lorenzo Livianos-Aldana hanno redatto il manoscritto. Tutti gli autori sono stati coinvolti nella preparazione della bozza del manoscritto, nella formulazione dei commenti sul manoscritto e nell’approvazione della versione finale dell’articolo.
Conflitto d’interessi
Gli autori dichiarano assenza di conflitto di interesse.
Riferimenti
- Jacka, F.N.; Kremer, P.J.; Leslie, E.R.; Berk, M.; Patton, G.C.; Toumbourou, J.W.; Williams, J.W. Associations between diet quality and depressed mood in adolescents: Results from the Australian Healthy Neighbourhoods Study. Aust. N. Z. J. Psychiatry 2010, 44, 435–442.
- Kessler, R.C.; Berglund, P.; Demler, O.; Jin, R.; Merikangas, K.R.; Walters, E.E. Lifetime prevalence and age-of-onset distributions of DSM-IV disorders in the National Comorbidity Survey Replication. Arch. Gen. Psychiatry 2005, 62, 593–602.
- Belfer, M.L. Child and adolescent mental disorders: The magnitude of the problem across the globe. J. Child Psychol. Psychiatry 2008, 49, 226–236.
- Hestetun, I.; Svendsen, M.V.; Oellingrath, I.M. Associations between overweight, peer problems, and mental health in 12–13-year-old Norwegian children. Eur. Child Adolesc. Psychiatry 2015, 24, 319–326.
- Bourre, J.M. Roles of unsaturated fatty acids (especially omega-3 fatty acids) in the brain at various ages and during ageing. J. Nutr. Health Aging 2004, 8, 163–174.
- Gomez-Pinilla, F. Brain foods: The effects of nutrients on brain function. Nat. Rev. Neurosci. 2008, 9, 568–578.
- Kulkarni, A.A.; Swinburn, B.A.; Utter, J. Associations between diet quality and mental health in socially disadvantaged New Zealand adolescents. Eur. J. Clin. Nutr. 2015, 69, 79–83.
- Adair, L.; Popkin, B. Are child eating patterns being transformed globally? Obes. Res. 2005, 13, 1281–1299.
- Nielsen, S.; Popkin, B. Patterns and trends in food portion sizes, 1977–1998. JAMA 2003, 289, 450–453.
- Nielsen, S.; Siega-Riz, A.; Popkin, B. Trends in energy intake in U.S. between 1977 and 1996: Similar shifts seen across age groups. Obes. Res. 2002, 10, 370–378.
- Wang, Z.; Zhai, F.; Du, S.; Popkin, B. Dynamic shifts in Chinese eating behaviors. Asia Pac. J. Clin. Nutr. 2008, 17, 123–130.
- Lobstein, T.; Baur, L.; Uauy, R. Obesity in children and young people: A crisis in public health. Obes. Rev.2004, 5, 4–85.
- Must, A.; Strauss, R.S. Risks and consequences of childhood and adolescent obesity. Int. J. Obes. Relat. Metab.Disord. 1999, 23, 2–11.
- McCrindle, B.W. Cardiovascular consequences of childhood obesity. Can. J. Cardiol. 2015, 31, 124–130.
- Maunder, E.M.; Nel, J.H.; Steyn, N.P.; Kruger, H.S.; Labadarios, D. Added sugar, macro- and micronutrient intakes and anthropometry of children in a developing world context. PLoS ONE 2015, 10, e0142059.
- 16. Collishaw, S.; Maughan, B.; Goodman, R.; Pickles, A. Time trends in adolescent mental health. J. Child Psychol. Psychiatry 2004, 45, 1350–1362.
- Twenge, J.M. Generational differences in mental health: Are children and adolescents suffering more, or less? Am. J. Orthopsychiatry 2011, 81, 469–472.
- West, P.; Sweeting, H. Fifteen, female and stressed: Changing patterns of psychological distress over time. J. Child Psychol. Psychiatry 2003, 44, 399–411.
- Jacka, F.N.; Kremer, P.J.; Berk, M.; de Silva-Sanigorski, A.M.; Moodie, M.; Leslie, E.R.; Pasco, J.A.; Swinburn, B.A. A prospective study of diet quality and mental health in adolescents. PLoS ONE 2011, 6, e24805.
- Oellingrath, I.M.; Svendsen, M.V.; Hestetun, I. Eating patterns and mental health problems in early adolescence–A cross-sectional study of 12–13-year-old Norwegian schoolchildren. Public Health Nutr. 2014, 17, 2554–2562.
- Weng, T.T.; Hao, J.H.; Qian, Q.W.; Cao, H.; Fu, J.L.; Sun, Y.; Huang, L.; Tao, F.B. Is there any relationship between dietary patterns and depression and anxiety in Chinese adolescents? Public Health Nutr. 2012, 15, 673–682.
- Morales-Suárez-Varela, M.; Rubio-López, N.; Ruso, C.; Llopis-Gonzalez, A.; Ruiz-Rojo, E.; Redondo, M.; Pico, Y. Anthropometric status and nutritional intake in children (6–9 years) in Valencia (Spain): The ANIVA Study. Int. J. Environ. Res. Public Health 2015, 12, 16082–16095.
- Barrett-Connor, E. Nutrition epidemiology: How do we know what they ate? Am. J. Clin. Nutr. 1991, 54, 182–187.
- Institute of Medicine (IOM). Dietary Reference Intakes: Applications in Dietary Assessment; National Academy Press: Washington, DC, USA, 2001.
- Ortega, R.M.; Requejo, A.M.; López-Sobaler, A.M. Modelos de cuestionarios para realización de estudios dietéticos en la valoración del estado nutricional. In Nutriguía Manual de Nutrición Clínica en Atención Primaria; Ortega, R.M., Requejo, A.M., Eds.; Editorial Complutense: Madrid, Spain, 2006; pp. 456–459. (In Spanish)
- Ortega, R.M.; Lopez, A.M.; Andrés, P.; Requejo, A.M.; Aparicio, A.; Molinero, L.M. DIAL Programa Para la Evaluación de Dietas y Gestión de Datos de Alimentación; Alce Ingeniería: Madrid, Spain, 2008. (In Spanish)
- Institute of Medicine (IOM). Dietary Reference Intakes: Applications in Dietary Assessment; National Academy Press: Washington, DC, USA, 2000.
- Institute of Medicine (IOM). Dietary Reference Intakes: Applications in Dietary Planning; National Academy Press: Washington, DC, USA, 2003.
- Murphy, S.P.; Barr, S.I. Practice paper of the American Dietetic Association: Using the dietary reference intakes. J. Am. Diet. Assoc. 2011, 111, 762–770.
- Sociedad Española de Nutrición Comunitaria (SENC). Objetivos nutricionales para la población española. Span. J. Community Nutr. 2001, 17, 178–199. (In Spanish)
- Federación Española de Sociedades de Nutrición, Alimentación y Dietética (FESNAD). Ingestas dietéticas de referencia (IDR) para la población española. Act. Diet. 2010, 14, 196–197. (In Spanish)
- Carriquiry, A.L. Assessing the prevalence of nutrient inadequacy. Public Health Nutr. 1999, 2, 23–33.
- World Health Organization Child Growth Standards: Length/Height-for-Age, Weight-for-Age, Weight-for-Length, Weight-for-Height and Body Mass Index for Age. 2006. Available online: http://www.who.int/childgrowth/standards/Technical_report.pdf (accessed on 17 December 2015).
- Onis, M.; Onyango, A.W.; Borghi, E.; Siyam, A.; Nishida, C.; Siekmann, J. Development of a WHO growth reference for school-aged children and adolescents. Bull. World Health Organ. 2007, 85, 660–667.
- World Health Organization OMS Anthro, a Software for Assessing Growth and Development of the World’s Children (Version 3.2.2). Available online: http://www.who.int/childgrowth/software/es/ (accessed on 20 March 2015).
- Centers for Disease Control and Prevention Defining Childhood Overweight and Obesity. Available online: http://www.cdc.gov/obesity/childhood/defining.html (accessed on 17 December 2015).
- Durnin, J.V.; Womersley, J. Body fat assessed from total body density and its estimation from skinfold thickness: measurements on 481 men and women aged from 16 to 72 years. Br. J. Nutr. 1974, 32, 77–97.
- 38. Faulstich, M.E.; Carey, M.P.; Ruggiero, L.; Enyart, P.; Gresham, F. Assessment of depression in childhood and adolescence: An evaluation of the Center for Epidemiological Studies Depression Scale for Children (CES-DC). Am. J. Psychiatry 1986, 143, 1024–1027.
- Najman, J.M.; Heron, M.A.; Hayatbakhsh, M.R.; Dingle, K.; Jamrozik, K.; Bor, W.; O’Callaghan, M.J.; Williams, G.M. Screening in early childhood for risk of later mental health problems: A longitudinal study. J. Psychiatry Res. 2008, 42, 694–700.
- Steinhausen, H.C.; Winkler Metzke, C. Prevalence of affective disorders in children and adolescents: Findings from the Zurich Epidemiological Studies. Acta Psychiatr. Scand. Suppl. 2013, 418, 20–23.
- Bernaras, E.; Jaureguizar, J.; Soroa, M.; Ibabe, I.; Cuevas, C. Evaluation of the depressive symptomatology and the related variables in the school context. An. Psicol. 2013, 29, 131–140.
- Angold, A.; Erkanli, A.; Silberg, J.; Eaves, L.; Costello, E.J. Depression scale scores in 8–17-year-olds: Effects of age and gender. J. Child Psychol. Psychiatry 2002, 43, 1052–1063.
- Costello, E.J.; Mustillo, S.; Erkanli, A.; Keeler, G.; Angold, A. Prevalence and development of psychiatric disorders in childhood and adolescence. Arch. Gen. Psychiatry 2003, 60, 837–844.
- Stringaris, A.; Maughan, B.; Copeland, W.S.; Costello, E.; Angold, A. Irritable mood as a symptom of depression in youth: Prevalence, developmental, and clinical correlates in the Great Smoky Mountains Study. J. Am. Acad. Child Adolesc. Psychiatry 2013, 52, 831–840.
- Maughan, B.; Rowe, R.; Messer, J.; Goodman, R.; Meltzer, H. Conduct disorder and oppositional defiant disorder in a national sample: Developmental epidemiology. J. Child Psychol. Psychiatry 2004, 45, 609–621.
- Chung, K.H.; Chiou, H.Y.; Chen, Y.H. Psychological and physiological correlates of childhood obesity in Taiwan. Sci. Rep. 2015, 5, 17439.
- Sanders, R.H.; Han, A.; Baker, J.S.; Cobley, S. Childhood obesity and its physical and psychological co-morbidities: A systematic review of Australian children and adolescents. Eur. J. Pediatr. 2015, 174, 715–746.
- Roohafza, H.; Kelishadi, R.; Sadeghi, M.; Hashemipour, M.; Pourmoghaddas, A.; Khani, A. Are obese adolescents more depressed? J. Educ. Health Promot. 2014, 3.
- Morrison, K.M.; Shin, S.; Tarnopolsky, M.; Taylor, V.H. Association of depression & health related quality of life with body composition in children and youth with obesity. J. Affect. Disord. 2014, 172C, 18–23.
- Kaner, G.; Soylu, M.; Yüksel, N.; Inanç, N.; Ongan, D.; Bas¸mısırlı, E. Evaluation of nutritional status of patients with depression. Biomed Res. Int. 2015, 2015.
- Serra-Majem, L.; Ribas-Barba, L.; Pérez-Rodrigo, C.; Bartrina, J.A. Nutrient adequacy in Spanish children and adolescents. Br. J. Nutr. 2006, 1, 49–57.
- Gibson, R.S. Evaluation of Nutrient Intake Data Principles of Nutritional Assessment; Oxford University Press: Oxford, UK, 1990.
- Henríquez-Sánchez, P.; Díaz-Romero, C.; Rodríguez-Rodríguez, E.; López-Blanco, F.; Alvarez-Leon, E.; Díaz-Cremades, J.; Pastor-Ferrer, M.C.; Serra-Majem, L. Evaluación bioquímica del estado nutricional de la población canaria (1997–1998). Arch. Latinoam. Nutr. 2000, 50, 43–54. (In Spanish).
- Oddy, W.H.; Robinson, M.; Ambrosini, G.L.; O’Sullivan, T.A.; de Klerk, N.H.; Beilin, L.J.; Silburn, S.R.; Zubrick, S.R.; Stanley, F.J. The association between dietary patterns and mental health in early adolescence. Prev. Med. 2009, 49, 39–44.
- O’Neil, A.; Quirk, S.E.; Housden, S.; Brennan, S.L.; Williams, L.J.; Pasco, J.A.; Berk, M.; Jacka, F.N. Relationship between diet and mental health in children and adolescents: A systematic review. Am. J. Public Health 2014, 104, e31–e42.
- Khosravi, M.; Sotoudeh, G.; Majdzadeh, R.; Nejati, S.; Darabi, S.; Raisi, F.; Esmaillzadeh, A.; Sorayani, M. Healthy and unhealthy dietary patterns are related to depression: A case-control study. Psychiatry Investig. 2015, 12, 434–442.
- Rao, T.S.; Asha, M.R.; Ramesh, B.N.; Rao, K.S. Understanding nutrition, depression and mental illnesses. Indian J. Psychiatry 2008, 50, 77–82.
- 58. Jéquier, E. Carbohydrates as a source of energy. Am. J. Clin. Nutr. 1994, 59, S682–S685.
- Harvey-Anderson, G. Carbohydrate, behavior and health. Bahrain Med. Bull. 1998, 20, 3.
- 60. Fang, C.Y.; Egleston, B.L.; Gabriel, K.P.; Stevens, V.J.; Kwiterovich, P.O.; Snetselaar, L.G.; Longacre, M.L.; Dorgan, J.F. Depressive symptoms and serum lipid levels in young adult women. J. Behav. Med. 2013, 36, 143–152.
- Blunden, C.H.; Inskip, H.M.; Robinson, S.M.; Cooper, C.; Godfrey, K.M.; Kendrick, T.R. Postpartum depressive symptoms: The B-vitamin link. Ment. Health Fam. Med. 2012, 9, 5–13.
- Kim, T.H.; Choi, J.Y.; Lee, H.H.; Park, Y. Associations between dietary pattern and depression in Korean adolescent girls. J. Pediatr. Adolesc. Gynecol. 2015, 28, 533–537.
- Coppen, A.; Bolander-Gouaille, C. Treatment of depression: Time to consider folic acid and vitamin B12. J. Psychopharmacol. 2005, 19, 59–65.
- Ataie-Jafari, A.; Qorbani, M.; Heshmat, R.; Ardalan, G.; Motlagh, M.E.; Asayesh, H.; Arzaghi, S.M.; Tajadini, M.H.; Nejatinamini, S.; Poursafa, P.; et al. The association of vitamin D deficiency with psychiatric distress and violence behaviors in Iranian adolescents: The CASPIAN-III study. J. Diabetes Metab. Disord. 2015, 14.
- Frusciante, L.; Carli, P.; Ercolano, M.R.; Pernice, R.; Di Matteo, A.; Fogliano, V.; Pellegrini, N. Antioxidant nutritional quality of tomato. Mol. Nutr. Food Res. 2007, 51, 609–617.
- 66. Kohatsu, W. Nutrition and depression. Explore 2005, 1, 474–476.
- Llewellyn, D.J.; Langa, K.M.; Lang, I.A. Serum 25-hydroxyvitamin D concentration and cognitive impairment. J. Geriatr. Psychiatry Neurol. 2009, 22, 188–195.
- German, L.; Kahana, C.; Rosenfeld, V.; Zabrowsky, I.; Wiezer, Z.; Fraser, D.; Shahar, D.R. Depressive symptoms are associated with food insufficiency and nutritional deficiencies in poor community-dwelling elderly people. J. Nutr. Health Aging 2011, 15, 3–8.
- Miki, T.; Kochi, T.; Eguchi, M.; Kuwahara, K.; Tsuruoka, H.; Kurotani, K.; Ito, R.; Akter, S.; Kashino, I.; Pham, N.M.; et al. Dietary intake of minerals in relation to depressive symptoms in Japanese employees: The Furukawa Nutrition and Health Study. Nutrition 2015, 31, 686–690.
- Lehto, S.M.; Ruusunen, A.; Tolmunen, T.; Voutilainen, S.; Tuomainen, T.P.; Kauhanen, J. Dietary zinc intake and the risk of depression in middle-aged men: A 20-year prospective follow-up study. J. Affect. Disord. 2013, 150, 682–685.
- Bodnar, L.M.; Wisner, K.L. Nutrition and depression: Implications for improving mental health among childbearing-aged women. Biol. Psychiatry 2005, 58, 679–685.
- Manios, Y.; Moschonis, G.; Mavrogianni, C.; Bos, R.; Singh-Povel, C. Micronutrient intakes among children and adults in Greece: The role of age, sex and socio-economic status. Nutrients 2014, 6, 4073–4092.
- Durá-Travé, T.; Gallinas-Victoriano, F. Dietary pattern among schoolchildren with normal nutritional status in Navarre, Spain. Nutrients 2014, 6, 1475–1487.



