Padala, Prasad R. MD, MS a,b,c,∗ ; Padala, Kalpana P. MD, MS a, c ; Majagi, Anusha S. BS a ; Garner, Kimberly K. MD a,c ; Dennis, Richard A. PhD a ; Sullivan, Dennis H. MD a, c
Pubblicato su Medicina 2020 – Volume 99 – Numero 33 – p e21497
Traduzione in italiano a cura del Dott. Claudio Ajmone per GiùleManidaiBambini.org
Testo originale in inglese, disponibile a questo link
a centro clinico e di educazione alla ricerca geriatrica, sistema sanitario per i veterani dell’Arkansas centrale
b Dipartimento di Psichiatria, Università dell’Arkansas per le scienze mediche (UAMS)
c Dipartimento di Geriatria, UAMS, Little Rock, AR, USA.
∗Corrispondenza: Prasad R. Padala, e-mail: Prasad.padala@va.gov
Estratto
Gli inibitori selettivi della ricaptazione della serotonina (SSRI), comunemente usati per trattare la depressione, sono associati a perdita di motivazione, anergia e mancanza di curiosità, spesso indicati collettivamente come apatia. Tuttavia, questa associazione non è stata valutata sistematicamente utilizzando una scala di valutazione specifica per misurare la sindrome da apatia. Il nostro obiettivo era studiare l’associazione tra l’uso di SSRI e la sindrome da apatia.
Abbiamo condotto una revisione retrospettiva del grafico di 125 pazienti arruolati in una clinica psichiatrica ambulatoriale. La prevalenza della sindrome da apatia e il suo significato clinico (basato su una valutazione standardizzata) sono stati confrontati tra i pazienti trattati e non trattati con SSRI. L’apatia è stata valutata utilizzando la versione clinica della scala di valutazione dell’apatia con un punteggio compreso tra 18 e 72 con un punteggio più alto per l’apatia peggiore. Un punteggio maggiore di 30 è considerato apatia clinicamente significativa.
Tra 119 pazienti, i punteggi medi di apatia erano significativamente più alti in quelli trattati con SSRI rispetto a quelli non trattati con SSRI (42,5 ± 9,2 vs 31,3 ± 6, P <0,0001). Il gruppo SSRI aveva anche una percentuale significativamente più alta di pazienti con apatia clinicamente significativa (92% vs 61%, P <.0001). L’uso di tutti gli SSRI è stato associato alla presenza di apatia. L’apatia è stata osservata in tutte le categorie diagnostiche di salute mentale con i punteggi più alti della versione clinica della scala di valutazione dell’apatia in quelli con demenza.
L’uso di SSRI può essere associato a tassi più elevati di sindrome da apatia. I medici dovrebbero informarsi specificamente sulla sindrome da apatia iatrogena quando valutano i pazienti su un SSRI se vi è il sospetto di perdita di motivazione. I limiti di questo studio includevano la natura retrospettiva di questo studio e la maggioranza del campione era costituita da maschi. Sono necessari studi prospettici per chiarire le informazioni riguardanti la prevalenza, l’eziologia e la risposta al trattamento per la sindrome da apatia associata a SSRI.
1. Introduzione
Ci si rende sempre più conto che l’apatia e la depressione sono entità distinte e separabili che possono rispondere in modo diverso a diversi farmaci. [1,2] La sindrome dell’apatia è una perdita primaria di motivazione indipendente da qualsiasi danno intellettivo, disagio emotivo o diminuzione della coscienza. [3] Spesso l’apatia passa inosservata a causa dell’indifferenza del paziente verso la sua situazione. La presenza di apatia è stata ben descritta in pazienti con disturbi neurocognitivi maggiori, schizofrenia e disturbo depressivo maggiore. Esiste un’ampia letteratura sui sintomi negativi della schizofrenia e un recente studio (N = 1208) con pazienti della European Schizophrenia Cohort aggiunge all’evidenza che la depressione potrebbe non mediare i sintomi negativi. [4]
I sintomi dell’apatia, come perdita di interesse, ritardo psicomotorio, anergia e mancanza di intuizione, possono essere erroneamente attribuiti a disturbi depressivi. [5] L’apatia ha un impatto diretto sullo stato funzionale dei pazienti anche dopo aver controllato l’effetto della depressione. In uno studio, i pazienti con apatia avevano una probabilità 3,2 volte maggiore di avere deficit nelle attività della vita quotidiana rispetto a quelli senza apatia. [6] L’ apatia può anche ostacolare il rispetto delle raccomandazioni terapeutiche. Il nostro gruppo ha scoperto che la presenza della sindrome da apatia, anche in assenza di depressione, era collegata a una scarsa compliance alla cura di sé per il diabete e a uno scarso controllo glicemico. [7] Diversi team, incluso il nostro, hanno scoperto che il trattamento dell’apatia è distinto dal trattamento della depressione. [8-10] Inoltre, la presenza di apatia aumenta il carico del caregiver. [11] Pertanto, è importante eseguire uno screening per l’apatia in contesti clinici.
Gli inibitori selettivi della ricaptazione della serotonina (SSRI) sono generalmente considerati un trattamento di prima linea per la depressione. Il loro uso è preferito rispetto ad altri agenti a causa del loro profilo di sicurezza relativamente favorevole e della facilità di somministrazione. Tuttavia, sono stati segnalati come potenziali effetti avversi di questi farmaci la diminuzione della gamma emotiva, la perdita di motivazione, la perdita di curiosità intellettuale, tutti componenti della sindrome da apatia. [12-16]L’associazione dell’apatia con l’uso di SSRI viene sempre più riconosciuta come un effetto di classe, a insorgenza rapida, reversibile con l’interruzione degli SSRI in alcuni casi e indipendentemente dall’età dei pazienti o dall’indicazione per l’uso degli SSRI.
In un campione di 181 pazienti con malattia di Parkinson, l’uso di SSRI ma nessun altro antidepressivo è stato associato ad apatia, indicando l’effetto di classe di questi farmaci. L’associazione è stata osservata anche dopo aver controllato i sintomi depressivi, l’età, l’istruzione, il sesso e l’uso di altri agenti psicotropi. [17] L’inizio dell’apatia con l’uso di SSRI può essere molto rapido. In uno studio su volontari sani, 1 settimana di utilizzo di citalopram è stata collegata a una riduzione dell’attività nelle reti di ricompensa dello striato ventrale e della corteccia ventrale mediale/orbitale.[18] l’apatia associata agli SSRI è osservata in pazienti con varie diagnosi tra cui depressione, disturbo di panico e disturbo ossessivo-compulsivo, il che suggerisce che l’associazione sia dovuta al farmaco piuttosto che alla diagnosi. [13]
Bolling et al hanno condotto interviste telefoniche semi-strutturate a pazienti che hanno completato una sperimentazione con antidepressivi e hanno scoperto che quasi il 20% dei 161 soggetti lamentava “apatia” e “perdita di creatività” sebbene non fosse stata eseguita alcuna valutazione specifica dell’apatia. [19] Sebbene la maggior parte di queste segnalazioni riguardi giovani adulti, Wongpakaran et al hanno riportato tale associazione nei pazienti geriatrici. In un’analisi post-hoc di un database ospedaliero, le sottoscale dell’apatia sono state derivate dalla Geriatric Depression Scale e dalle Hamilton Depression Scales aggiungendo elementi pertinenti all’apatia. [20] Hanno separato 384 soggetti in 2 gruppi in base all’uso di SSRI e hanno scoperto che l’apatia era più prevalente per i pazienti che assumevano SSRI rispetto a non assumevano SSRI. [20]
Nessuno di questi studi fino ad oggi ha utilizzato scale di valutazione convalidate per valutare specificamente l’apatia associata all’uso di SSRI. La versione Apathy Evaluation Scale-Clinician (AES-C) è una scala di 18 item in grado di catturare l’apatia come sindrome e differenziarla dalla depressione. [21] Lo scopo dell’attuale revisione retrospettiva del grafico era di utilizzare una scala di apatia convalidata per indagare su un’eventuale associazione tra l’apatia e l’uso di farmaci SSRI. Volevamo anche verificare se l’associazione dell’uso di SSRI con l’apatia differiva dallo specifico SSRI. Abbiamo ipotizzato che la sertralina possa avere meno probabilità di essere associata all’apatia a causa delle sue azioni dopaminergiche.
2. Metodi
È stata ottenuta l’approvazione dall’Institutional Review Board per interrogare un database clinico che incorpora misure di esito convalidate basate sull’evidenza per questa revisione del grafico. Sono stati esaminati i grafici di 125 pazienti consecutivi della Clinica di salute mentale, della Clinica di psichiatria geriatrica e del Centro di recupero presso il centro medico Veterans Affairs affiliato all’Università. Sono stati registrati dati demografici tra cui età, diagnosi di salute mentale e farmaci. Quando c’erano più di 1 diagnosi di salute mentale, è stata scelta 1 diagnosi primaria ai fini di questo documento, in base ai sintomi di presentazione nella visita indice e al carico complessivo causato dalla diagnosi. Sebbene in questo campione non sia stata ottenuta una scala di valutazione per la gravità della depressione, tra quelli con MDD, la gravità dell’episodio di depressione attuale è stata acquisita dalle cartelle cliniche.
La sindrome da apatia è stata accertata dai punteggi dell’AES-C. [20] L’AES-C è una scala di 18 elementi che valuta l’iniziativa, la motivazione, la persistenza e altri aspetti dell’apatia di un paziente, tutti valutati su una scala Likert a 4 punti. AES-C cattura gli aspetti comportamentali, cognitivi ed emotivi dell’apatia. I punteggi totali vanno da 18 a 72 con punteggi più alti che indicano una peggiore apatia. Tre elementi hanno una sintassi negativa per garantire la validità delle risposte. L’AES-C è stato testato in vari disturbi neurodegenerativi e ha una buona consistenza interna (coefficiente alfa = .86) e affidabilità test-retest (r = .76). [21] La versione somministrata dal medico è nota per differenziare in modo affidabile l’apatia dalla depressione. [21] Un punteggio superiore a 30 sull’AES-C è generalmente considerato indicare un’apatia clinicamente significativa. [21]
L’analisi della varianza è stata eseguita per confrontare i punteggi AES-C in entrambi i gruppi. L’analisi chi-quadrato è stata utilizzata per confrontare la percentuale di pazienti in ciascun gruppo con apatia clinicamente significativa (AES-C > 30). Il test Chi-Square è stato eseguito anche sul numero di pazienti che utilizzano SSRI specifici. Il test Fisher Exact è stato utilizzato quando N ≤ 5 in qualsiasi cella.
3. Risultati
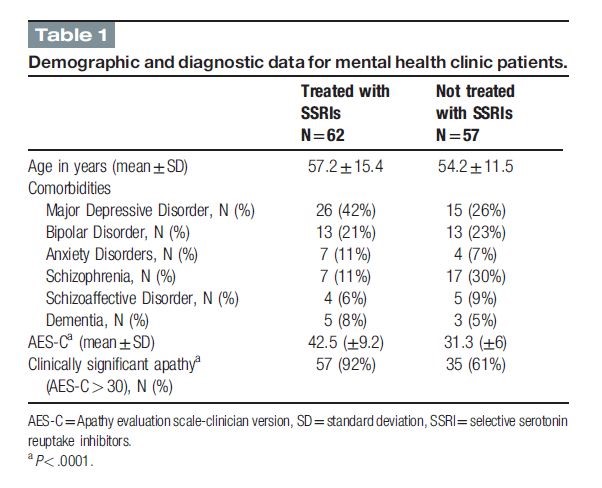
Delle 125 cartelle cliniche esaminate, 6 sono state escluse per mancanza di informazioni sulla diagnosi e/o sui farmaci. L’età media dei 119 pazienti inclusi nell’analisi era 55,8 ± 13,6 (deviazione standard) anni e il punteggio medio AES-C era 37,13 ± 9,5. Il disturbo depressivo maggiore è stata la diagnosi più comune nel campione, seguita da disturbo bipolare e schizofrenia ( Tabella 1 ). Sessantadue pazienti (52%) erano in trattamento con SSRI. I pazienti non trattati con SSRI erano più giovani di quelli trattati con SSRI, ma la differenza non era statisticamente significativa [(54,2 ± 11,5) vs (57,2 ± 15,4)] ( Tabella 1). Il gruppo SSRI ha avuto una tendenza verso una percentuale maggiore di disturbo depressivo maggiore rispetto al gruppo non SSRI (42% vs 26%, P< .07), oltre ad avere una percentuale significativamente inferiore di pazienti con schizofrenia (11% vs 30%, P < .01) (Tabella 1).
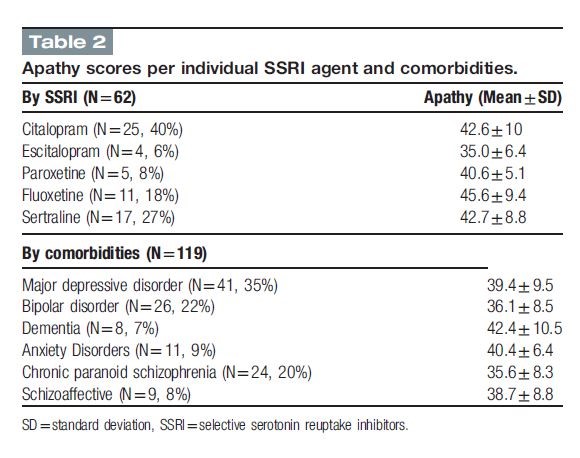
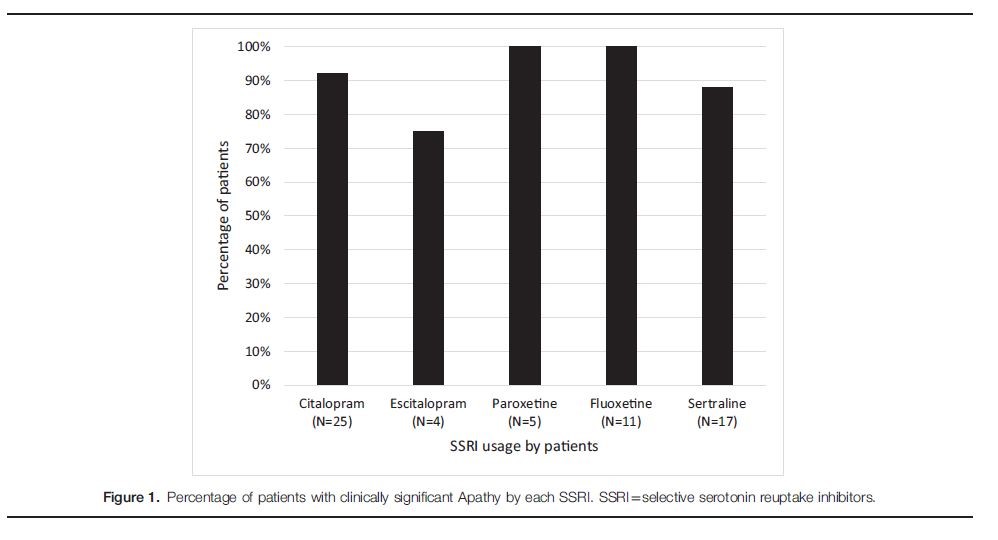
Il gruppo SSRI aveva punteggi significativamente più alti sull’AES-C (42,5 ± 9,2 vs 31,3 ± 6, P < 0,0001) e una percentuale significativamente più alta di pazienti con apatia clinicamente significativa (punteggi AES-C > 30) (92% vs 61%, P <.0001) rispetto al gruppo non SSRI. I punteggi AES-C sono stati analizzati dai singoli SSRI. Il numero di pazienti che ricevono diversi tipi di SSRI è elencato nella Tabella 2 . Tutti e 5 gli agenti sono stati associati a punteggi elevati sull’AES-C che vanno da 35 ± 6,4 per il gruppo escitalopram a 45,6 ± 9,4 con il gruppo fluoxetina ( Tabella 2). La maggior parte dei pazienti trattati con questi agenti presentava un’apatia clinicamente significativa che variava dal 75% nel gruppo escitalopram al 100% con paroxetina e fluoxetina (Fig. 1).
Apatia clinicamente significativa è stata osservata in tutte le diagnosi psichiatriche con i punteggi più alti osservati nei pazienti con demenza, seguita da disturbi d’ansia e disturbo depressivo maggiore ( Tabella 2). Il punteggio medio AES-C era più basso nel MDD-grave (N = 29) (38,4 ± 9,8) rispetto al gruppo con MDD moderato e lieve combinato (N = 12) (41,3 ± 9,3) (p = 0,39). La percentuale di apatia clinicamente significativa era del 100% in quelli con demenza, seguita da ansia (93%) e MDD (80%). Il punteggio medio di apatia era il minimo nei pazienti con schizofrenia paranoide cronica (35,6 ± 8,3). In questo sottogruppo, non c’era alcuna differenza statisticamente significativa nei punteggi di apatia tra quelli su SSRI rispetto a quelli non su SSRI ( P = 0,54).
4. Discussione
Nel presente studio, i pazienti in trattamento con SSRI avevano punteggi di apatia più alti rispetto a quelli che non stavano assumendo SSRI. La maggior parte dei pazienti trattati con SSRI (92%) presentava un’apatia clinicamente significativa, il che suggerisce che i punteggi elevati sull’AES-C non erano influenzati da pochi valori anomali. Ciò supporta i precedenti rapporti sulla sindrome da apatia associata all’uso di SSRI. [12-19] Il nostro studio si differenzia dai precedenti studi sull’apatia poiché abbiamo valutato l’apatia come una sindrome piuttosto che come un sintomo. Abbiamo anche utilizzato una scala di valutazione convalidata specificamente progettata per differenziare la sindrome dell’apatia dalla depressione.
Il fatto che in questo rapporto siano stati osservati punteggi elevati su AES-C con tutti gli SSRI suggerisce un’associazione della sindrome da apatia con gli SSRI come classe. È possibile che la maggiore proporzione di MDD nel gruppo SSRI possa in parte spiegare l’associazione con l’apatia. Mentre parte dell’associazione è spiegata dalla sovrapposizione della sintomatologia tra depressione e apatia, la differenza nei punteggi di apatia tra i gruppi potrebbe non essere spiegata completamente dalla sovrapposizione fenomenologica. Ad esempio, una differenza di 3,3 punti su AES-C è generalmente considerata una differenza clinicamente significativa e, in questo campione,[8] L’attuale letteratura sull’apatia indotta da SSRI è dominata principalmente da case report e il nostro studio conferma i risultati dell’apatia indotta da SSRI con un campione di grandi dimensioni rispetto alla ricerca esistente.
Abbiamo ipotizzato che la sertralina con alcune lievi proprietà di inibizione della ricaptazione della dopamina oltre all’attività SSRI potrebbe avere meno probabilità di essere associata a punteggi di apatia elevati; tuttavia, non abbiamo riscontrato che ciò sia vero nella nostra popolazione. L’apatia può derivare da una serie di eziologie diverse. Studi su pazienti in seguito a lesioni cerebrali dimostrano che l’apatia deriva da un danno alle aree paralimbiche prefrontali mediali, cingolate anteriori e temporali anteriori come l’amigdala. [22] Anche gli ictus che coinvolgono l’arto posteriore della capsula interna possono causare apatia. [23] L’apatia è un disturbo comportamentale frequente nella demenza di Alzheimer (AD). Gli studi di tomografia computerizzata a emissione di singolo fotone di pazienti con AD hanno rivelato una diminuzione della perfusione nelle regioni anteriori nei pazienti apatici e nelle regioni posteriori dei pazienti senza apatia. [24] Questi risultati supportano il suggerimento che i meccanismi neurali dell’apatia coinvolgano i circuiti del tronco cerebrale e del proencefalo che mediano il comportamento finalizzato.
È noto anche che l’anomalia dopaminergica causa apatia. La sindrome dell’apatia è stata segnalata dopo un danno alla corteccia cingolata anteriore che riceve un ampio input dopaminergico dall’area tegmentale ventrale. Hoehn-Saric et al offrono un modello plausibile che suggerisce un duplice impatto degli SSRI sulla corteccia frontale, 1 tramite il sistema serotoninergico e l’altro tramite la modulazione indiretta dei sistemi dopaminergici del mesencefalo che si proiettano sulla corteccia prefrontale. [15] Questo stato ipodopaminergico indotto da SSRI porta a sintomi di apatia. Inoltre, è stato riportato che gli agenti dopaminergici, come il metilfenidato, trattano l’apatia indipendentemente dalla depressione. [9,10,25,26] Un meccanismo simile potrebbe spiegare la fisiopatologia dei sintomi extrapiramidali associati agli SSRI.
In 1 caso clinico di apatia indotta da SSRI (fluoxetina), è stata osservata una diminuzione del flusso sanguigno nei lobi frontali insieme a un peggioramento dell’apatia. Questi risultati sono stati annullati con l’interruzione della fluoxetina. [15] L’ apatia indotta da SSRI sembra quindi essere dose e durata dipendente, oltre che reversibile. [12-16] Il nostro team ha pubblicato un rapporto a sostegno della reversibilità della sindrome da apatia associata a SSRI con l’interruzione o la riduzione del dosaggio dell’agente. [27]
I limiti di questo studio includono, ma non sono limitati a, la natura retrospettiva di questo studio, la mancanza di cecità dei revisori allo stato SSRI, la mancanza di una valutazione di fattori psicosociali confondenti, fattori di uso di sostanze o una valutazione di malattie mediche in corso e in peggioramento . Le differenze nelle categorie diagnostiche, come i disturbi più affettivi nel gruppo SSRI, potrebbero aver avuto un impatto sui punteggi di apatia. Tuttavia, nel gruppo non SSRI, i punteggi di apatia erano bassi nonostante la percentuale più alta di pazienti con schizofrenia noti per sintomi negativi. È interessante notare che nella sottoanalisi dei pazienti con schizofrenia non è stata trovata alcuna associazione statisticamente significativa tra apatia e uso di SSRI, forse a causa del piccolo numero di pazienti in terapia con SSRI in questo sottocampione.
Non abbiamo potuto analizzare gli effetti di genere nel nostro campione poiché solo 8 partecipanti erano donne a causa dell’impostazione del Department of Veterans Affairs. La prevalenza dell’apatia negli uomini anziani è una scoperta importante in quanto può essere associata al calo del testosterone.[28] Nonostante queste limitazioni, i nostri dati suggeriscono che gli SSRI possono essere correlati alla presenza di apatia. Altri studi suggeriscono che l’apatia migliora dopo l’interruzione degli SSRI o l’aumento con agenti dopaminergici come il bupropione. Sono necessari studi prospettici per identificare gli effetti degli SSRI nell’insorgenza e nel peggioramento dell’apatia nei pazienti con depressione e altre diagnosi psichiatriche.
5. Conclusioni
Questo studio indica che esiste un’associazione tra l’uso di SSRI e la sindrome da apatia concomitante. Convalida ulteriormente che l’associazione può essere vera per tutti gli SSRI e può essere vista in varie condizioni di salute mentale. Sono necessari studi prospettici per chiarire le informazioni riguardanti se lo sviluppo della sindrome di apatia è causalmente correlato all’inizio della terapia con un SSRI, nonché la prevalenza, l’eziologia e la risposta al trattamento per la sindrome da apatia associata a SSRI.
Contributi dell’autore
Concettualizzazione: Prasad R. Padala.
Analisi dei dati: Prasad R. Padala.
Interpretazione delle analisi: Kalpana P. Padala, Dennis H. Sullivan.
Indagine: Kalpana P. Padala.
Interviste ai pazienti: Prasad R. Padala.
Approvazioni normative: Prasad R. Padala.
Convalida: Anusha S. Majagi.
Scrittura – bozza originale: Prasad R. Padala, Kalpana P. Padala, Anusha S. Majagi, Kimberly K. Garner, Richard A. Dennis, Dennis H. Sullivan.
Riferimenti
- Levy ML, Cummings JL, Fairbanks LA, et al. Apathy is not depression. J Neuropsychiatry Clin Neurosci 1998;10:314–9.
- Padala PR, Petty F, Bhatia SC. Methylphenidate may treat apathy independent of depression. Ann Pharmacother 2005;39:1947–9.
- Marin RS. Differential diagnosis and classification of apathy. Am J Psychiatry 1990;147:22–30.
- Carrà G, Crocamo C, Bartoli F, et al. The mediating role of depression in pathways linking positive and negative symptoms in schizophrenia. A longitudinal analysis using latent variable structural equation modelling. Psychol Med 2020;50:566–74.
- Marin RS, Firinciogullari S, Biedrzycki RC. The sources of convergence between measures of apathy and depression. J Affect Disord 1993;28:117–24.
- Freels S, Cohen D, Eisdorfer C, et al. Functional status and clinical findings in patients with Alzheimer’s disease. J Gerontol 1992;47:M177–82.
- Padala PR, Desouza CV, Almeida S, et al. The impact of apathy on glycemic control in diabetes: a cross-sectional study. Diabetes Res Clin Pract 2008;79:37–41.
- Lanctot KL, Chau SA, Herrmann N, et al. Effect of methylphenidate on attention in apathetic AD patients in a randomized, placebo-controlled trial. Int Psychogeriatr 2014;26:239–46.
- Padala PR, Padala KP, Lensing SY, et al. Methylphenidate for Apathy in Community-Dwelling Older Veterans With Mild Alzheimer’s Disease: A Double-Blind, Randomized, Placebo-Controlled Trial. Am J Psychiatry 2017;175:159–68.
- Rosenberg PB, Lanctot KL, Drye LT, et al. Safety and efficacy of methylphenidate for apathy in Alzheimer’s disease: a randomized, placebo-controlled trial. J Clin Psychiatry 2013;74:810–6.
- Thomas P, Clement JP, Hazif-Thomas C, et al. Family, Alzheimer’s disease and negative symptoms. Int J Geriatr Psychiatry 2001;16:192–202.
- Barnhart WJ, Makela EH, Latocha MJ. SSRI-induced apathy syndrome: a clinical review. J Psychiatr Pract 2004;10:196–9.
- Garland EJ, Baerg EA. Amotivational syndrome associated with selective serotonin reuptake inhibitors in children and adolescents. J Child. Adolesc Psychopharmacol 2001;11:181–6.
- George MS, Trimble MR. A fluvoxamine-induced frontal lobe syndrome in a patient with comorbid Gilles de la Tourette’s syndrome and obsessive compulsive disorder. J Clin Psychiatry 1992;53:379–80.
- Hoehn-Saric R, Harris GJ, Pearlson GD, et al. A fluoxetine-induced frontal lobe syndrome in an obsessive compulsive patient. J Clin Psychiatry 1991;52:131–3.
- Hoehn-Saric R, Lipsey JR, McLeod DR. Apathy and indifference in patients on fluvoxamine and fluoxetine. J Clin Psychopharmacol 1990;10:343–5.
- Zahodne LB, Bernal-Pacheco O, Bowers D, et al. Are selective serotonin reuptake inhibitors associated with greater apathy in Parkinson’s disease? J Neuropsychiatry Clin Neurosci 2012;24:326–30.
- McCabe C, Mishor Z, Cowen PJ, et al. Diminished neural processing of aversive and rewarding stimuli during selective serotonin reuptake inhibitor treatment. Biol Psychiatry 2010;67:439–45.
- Bolling MY, Kohlenberg RJ. Reasons for quitting serotonin reuptake inhibitor therapy: paradoxical psychological side effects and patient satisfaction. Psychother Psychosom 2004;73:380–5.
- Wongpakaran N, van RR, Wongpakaran T, et al. Selective serotonin reuptake inhibitor use associates with apathy among depressed elderly: a case-control study. Ann Gen Psychiatry 2007;6:7.
- Marin RS, Biedrzycki RC, Firinciogullari S. Reliability and validity of the Apathy Evaluation Scale. Psychiatry Res 1991;38:143–62.
- Marin RS. Apathy: concept, syndrome, neural mechanisms, and treatment. Semin Clin Neuropsychiatry 1996;1:304–14.PubMed
- Starkstein SE, Fedoroff JP, Price TR, et al. Apathy following cerebrovascular lesions. Stroke 1993;24:1625–30.
- Benoit M, Koulibaly PM, Migneco O, et al. Brain perfusion in Alzheimer’s disease with and without apathy: a SPECT study with statistical parametric mapping analysis. Psychiatry Res 2002;114:103–11.
- Lanctot KL, Herrmann N, Black SE, et al. Apathy associated with Alzheimer disease: use of dextroamphetamine challenge. Am J Geriatr Psychiatry 2008;16:551–7.
- Padala PR, Burke WJ, Shostrom VK, et al. Methylphenidate for apathy and functional status in dementia of the Alzheimer type. Am J Geriatr Psychiatry 2010;18:371–4.
- Padala PR, Padala KP, Monga V, et al. Reversal of SSRI-associated apathy syndrome by discontinuation of therapy. Ann Pharmacother 2012;46:e8.
- Brodaty H, Altendorf A, Withall A, et al. Do people become more apathetic as they grow older? A longitudinal study in healthy individuals. Int Psychogeriatr 2010;22:426–36.