Ori Kapra 1 , Ran Rotem 2,3 e Raz Gross 1,4,5
Pubblicato su Frontiers in Paychiatry, 2020, Vol 11, article 555740
Traduzione in italiano a cura del Dott. Claudio Ajmone per GiùleManidaiBambini.org
Testo originale in inglese, disponibile a questo link
1 Department of Epidemiology and Preventive Medicine, Sackler Faculty of Medicine, School of Public Health, Tel Aviv University, Tel-Aviv, Israel,
2 School of Public Health, Harvard University, Boston, MA, United States,
3 Morris Kahn Maccabi Health Data Science Institute, Tel-Aviv, Israel,
4 Sheba Medical Center, Ramat Gan, Israel,
5Department of Psychiatry, Sackler Faculty of Medicine, Sackler School of Medicine, Tel Aviv University, Tel Aviv, Israel
L’uso di antidepressivi (AD) in generale, e nonostante la gravidanza, è aumentato a livello globale negli ultimi decenni. Associazioni con una vasta gamma di esiti avversi perinatali e infantili a seguito di esposizione prenatale ad AD sono state osservate in studi basati sul registro, con disturbi dello spettro autistico (ASD) frequentemente segnalati. Gli studi che utilizzano modelli animali, analisi dei fratelli e approcci di controllo negativo, hanno collegato il metabolismo disfunzionale della serotonina con l’ASD, ma non hanno distinto in modo convincente il ruolo della salute mentale materna da quello degli AD. Mentre il lavoro per decifrare la natura dell’associazione AD-ASD continua, questa revisione solleva alcuni problemi di salute pubblica pertinenti a una conclusione ipotetica che questa associazione sia causale, inclusa la necessità di identificare periodi di gestazione specifici con rischio più elevato, l’importanza di una valutazione precisa di la potenziale prevenzione dell’ASD che potrebbe essere attribuita all’interruzione dell’AD e la stima dei rischi associati all’esposizione prenatale alla depressione non trattata.
Parole chiave: autismo (ASD), antidepressivo (AD), SSRI (inibitore selettivo della ricaptazione della serotonina), depressione prenatale, materna, confondente per indicazione, sviluppo in utero.
1. Introduzione
L’uso di antidepressivi (AD) in gravidanza provoca l’esposizione del feto ai farmaci, in concentrazioni che sono il 70-80% dei livelli sierici materni (1). Tuttavia, l’esposizione del feto agli AD non ha ricevuto la stessa attenzione clinica, etica o sociologica degli AD usati nei bambini e negli adolescenti. Da una prospettiva etica e di ricerca sulla salute pubblica, questo argomento introduce alcune questioni chiave. In primo luogo, a differenza dei bambini e degli adolescenti che sono generalmente trattati seguendo il principio medico del primum non nocere (“Primo non nuocere”), vale a dire, trattando solo coloro che hanno dimostrato una compromissione sufficiente in modo tale che i benefici del trattamento superino i potenziali danni causati dagli effetti avversi, i feti sono “spettatori innocenti”, esposti passivamente all’AD. Ciò che è evidente negli studi suggeriscono che l’uso di inibitori selettivi della ricaptazione della serotonina (SSRI), una classe di AD, è aumentata globalmente negli ultimi 20-30 anni, in particolare tra le donne in gravidanza e (2-8).
In secondo luogo, le scelte che i medici e le donne in gravidanza che lottano con problemi di salute mentale sono complessi, in quanto in una difformità altre esposizioni come il tabacco o droghe illecite in cui l’obiettivo è quello di eliminare l’uso in gravidanza del tutto eliminando l’uso di SSRI e lasciando la depressione materna maggiore non trattata ha conseguenze deleterie sia per la madre che il bambino (9-11). Quindi, in qualche modo notevole per le indagini sull’esposizione prenatale all’AD, e agli SSRI in particolare, è un’equivocità epidemiologica sul fatto che si debba cercare il numero necessario per nuocere (NNH) o il numero necessario per il trattamento (NNT). Nell’ultimo decennio, questa ambiguità concettuale non ha scoraggiato la creazione di un’associazione coerente con un altro problema di salute pubblica, vale a dire il disturbo dello spettro autistico (ASD) (12,13).
L’associazione tra SSRI prenatali e disturbo dello spettro autistico (ASD)
Studi sui gemelli hanno proposto che fino al 70% delle coppie monozigoti sono concordi per l’autismo, mentre fino al ~ 90% sono concordi per uno spettro più ampio di anomalie cognitive o sociali correlate (14,15). Questi dati sull’ereditabilità suggeriscono che l’ASD è in gran parte genetico, fornendo al contempo prove sostanziali che anche i fattori non ereditabili possono avere un ruolo eziologico (16). Spesso menzionato tra queste le esposizioni prenatali è l’uso di farmaci SSRI.
Si sospetta che l’esposizione fetale agli SSRI abbia conseguenze significative, principalmente perché ben prima di assumere il suo rinomato ruolo di neurotrasmettitore in età adulta, la serotonina (5-HT) funge da fattore di crescita neurale durante la gestazione, influenzando in modo critico la struttura e la funzione del cervello il feto in via di sviluppo (17-22). Tutti gli SSRI attraversano la placenta e, sebbene il meccanismo mediante il quale gli SSRI possono diventare potenzialmente pericolosi durante la gestazione non sia del tutto chiaro, sono state osservate associazioni con un’ampia gamma di problemi perinatali avversi, tra cui una ridotta crescita della testa fetale (23), basso peso alla nascita (24), difetti del tubo neurale (25,26), malformazioni cardiache (27), in particolare difetti atriali e ventricolari (28), craniosinostosi (28), ipertensione polmonare persistente (29,30) e punteggi APGAR inferiori (31).
Tra i disturbi neuropsichiatrici infantili, l’ASD è stato associato all’esposizione prenatale agli SSRI (32). Figura 1 mostra che negli ultimi dieci anni studi osservazionali hanno formato un aggregato di risultati positivi, con poche, se ce ne sono, varietà nelle loro stime di effetto (33-49). Una meta analisi ha suggerito un odds ratio aggregato di 1,82, con un intervallo di confidenza (CI) del 95% = 1,59-2,10 (32) quando si confrontano feti esposti e non esposti, o un odds ratio aggiustato di 1,81 (IC 95% = 1,47-2,24) con eterogeneità non significativa delle stime degli effetti tra gli studi (rispettivamente: Q = 3,61, P = 0,73; Q = 0,5, P = 0,92) (45). Solo una singola meta-analisi fino ad oggi ha prodotto risultati nulli per l’associazione ASD-SSRI (RR aggiustato = 1,13, IC 95% = 0,93-1,39) (50). Questo risultato nullo è stato interpretato dagli autori come un fallimento di altre meta-analisi nel tenere conto del bias di pubblicazione. L’ultima revisione sistematica e la meta-analisi comprendente 20 studi avevano calcolato gli Hazard Ratio (HR) aggregati positivi per entrambi i disegni di coorte e caso-controllo (rispettivamente: HR = 1,27, IC 95% = 1,10-1,47; HR = 1,60, 95% CI = 1,26-2,02), e allo stesso modo ha richiamato l’attenzione sul fatto che non si può escludere che un bias di pubblicazione influenzi i risultati (40). Tuttavia, l’associazione osservata tra SSRI e disturbi dello sviluppo è attualmente difficilmente in discussione. La possibile causalità da essa implicita, tuttavia, è discutibile.
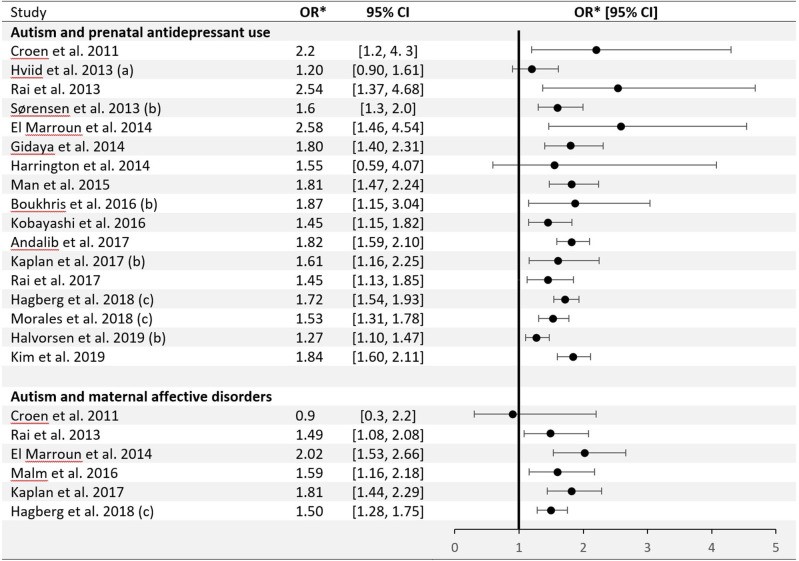
Sono emerse diverse strategie investigative per valutare la causalità dell’associazione tra l’uso materno di AD durante la gravidanza e il rischio di ASD nella progenie. I risultati di studi su modelli animali hanno rafforzato l’ipotesi che l’esposizione precoce SSRI può alterare il normale sviluppo del cervello, la neurogenesi ippocampale, e la programmazione epigenetica (51-55). Negli esseri umani, i campioni epidemiologici sono stati studiati mediante diversi approcci analitici, ognuno dei quali presenta sfide uniche. Modelli di regressione aggiustati per la malattia mentale della madre sono limitati a causa della sottostima stabilita di depressione (30,56-60), il che porta a un controllo incompleto del fattore confondente per indicazione o per gravità della depressione, con quest’ultimo che potenzialmente confonde anche il gradiente dose-risposta tra esposizione a SSRI e rischio di ASD. Limitare l’analisi solo a bambini nati da madri con una storia di disturbi psichiatrici sembra infatti attenuare o annullare l’associazione SSRI-ASD (3), come osservato in una revisione sistematica (46) e una meta-analisi (39) (rispettivamente: rapporto di rischio aggregato aggiustato = 1,18, 9 %% CI = 0,91-1,52; rapporto di rischio aggregato = 0,96, 95% CI = 0,57-1,6).
Figura 1 mostra anche studi che dimostrano un’associazione tra disturbi affettivi materni e ASD, incondizionata sull’uso di SSRI. La prima e unica meta-analisi per raccogliere dati su madri con solo disturbi psichiatrici ma senza esposizione a SSRI e quelle con esposizione a SSRI durante la gravidanza ha mostrato un rischio elevato di ASD in entrambi i gruppi (38). Un metodo aggiuntivo per tenere conto del confondimento da fonti genetiche o ambientali è l’analisi dei fratelli discordanti (all’esposizione) (61). È importante riconoscere, tuttavia, che i risultati degli studi di confronto tra fratelli possono essere distorti se ci sono fattori di confondimento non condivisi e variabili nel tempo tra fratelli (62), come osservato in uno studio particolare (49). I metodi di controllo negativo sono stati utilizzati a due livelli predominanti: uso pre-concepimento di SSRI (36,38) e uso paterno di SSRI (40,63). Dato il complicato modello di utilizzo degli SSRI e la variabilità degli stati depressivi nel tempo, questi approcci potrebbero non essere sempre validi (36).
In sintesi, degli approcci empirici per valutare il contributo dell’esposizione prenatale agli SSRI all’ASD, nessuno è riuscito in modo definitivo a separare il ruolo della depressione materna da quello del trattamento medicinale. I dati sono tuttavia altamente congruenti con un meccanismo biologico proposto di sviluppo di ASD, disfunzioni del metabolismo della serotonina e cambiamenti serotoninergici (64,65). Oltre alle limitazioni descritte nell’affrontare il bias di indicazione, l’ esposizione a SSRI in utero può potenzialmente intervenire anche con la diagnosi dell’end-point (66). I meccanismi che hanno un impatto sulla 5-HT negli adulti possono durare dopo l’interruzione del trattamento e possono potenzialmente alterare la funzione affettiva e cognitiva nei neonati e nei bambini che dipingono un quadro clinico specifico senza necessariamente causare autismo.
Discussione
È plausibile che presto saremo in grado di rispondere alla domanda “può l’esposizione prenatale agli SSRI causare ASD?” con un maggior grado di certezza, tuttavia la natura causale di questa associazione non affronta questo argomento di salute pubblica nella sua interezza. In primo luogo, i potenziali rischi di esposizione agli SSRI devono essere valutati considerando anche i potenziali effetti della depressione materna non trattata sul feto. Un ambiente intrauterino alterato a causa degli effetti correlati alla depressione materna sull’attività ipotalamo-ipofisi-surrenalica (HPA) è stato collegato a esiti avversi dello sviluppo neurologico (10). In secondo luogo, anche se si raggiunge un consenso scientifico sul fatto che gli SSRI sianodannosi per il feto, è improbabile che i farmaci comportino un rischio costante durante l’intera gravidanza e dovrebbero essere identificati i periodi critici di gestazione durante i quali il feto è potenzialmente più vulnerabile. Alcuni studi hanno associato un elevato rischio di ASD con l’esposizione agli SSRI nel primo trimestre (34,38,67), mentre altri hanno collegato gli effetti avversi con l’uso di SSRI nel secondo o terzo trimestre (45).
Evidenziando quanto sopra, una recente meta-analisi ha stabilito che, indipendentemente dall’esposizione agli SSRI del primo trimestre, gli effetti si osservano anche con l’esposizione del secondo trimestre (40). In terzo luogo, nel caso (attualmente ipotetico) in cui si trova una relazione causale, prima di considerare la modifica della categoria di sicurezza della gravidanza per gli SSRI, si raccomanda di avere una stima corretta della prevenzione proporzionale di ASD che potrebbe essere attribuita alla sospensione di SSRI, che poiché attualmente gli stand risultano essere molto modesti. Si stima che tra lo 0,6 e il 2% dei casi di ASD negli studi di coorte basati sulla popolazione avrebbe potuto essere prevenuto se l’esposizione prenatale agli SSRI fosse stata eliminata (36,48). Queste stime confutano i suggerimenti che la tendenza all’aumento della prevalenza di ASD sia attribuibile in modo significativo all’aumento dell’uso di farmaci per l’AD.
La percezione da parte della singola donna incinta del potenziale rischio associato con le esposizioni in-utero sono note per essere percepite come maggiori di quanto non siano in realtà (68). Tuttavia, una politica sanitaria pubblica equilibrata e un processo decisionale clinico sull’uso dell’AD durante la gravidanza porterebbero probabilmente a migliori risultati di salute sia per la madre che per la prole.
In conclusione, c’è poca contesa sul fatto che gli SSRI siano associati all’ASD. Nessuno studio fino ad oggi, tuttavia, ha escluso in modo convincente la possibilità di confondere o di indicare altri fattori. Poiché i dati accumulati su questo argomento supportano che il metabolismo della serotonina può essere nella via causale dell’ASD, sono necessari nuovi approcci che potrebbero chiarire questo enigma (69).
Contributi dell’autore
OK e RG hanno ideato il lavoro e redatto l’articolo. RR ha fornito suggerimenti critici per le revisioni.
Conflitto d’interesse
Gli autori dichiarano che la ricerca è stata condotta in assenza di rapporti commerciali o finanziari che potrebbero essere interpretati come un potenziale conflitto di interessi.
Riferimenti
- Hendrick V, Stowe ZN, Altshuler LL, Hwang S, Lee E, Haynes D. Placental passage of antidepressant medications. Am J Psychiatr. (2003) 160:993–6.
- Cooper WO, Willy ME, Pont SJ, Ray WA. Increasing use of antidepressants in pregnancy. Am J Obstet Gynecol. (2007) 196:544 e1–5.
- Jimenez-Solem E, Andersen JT, Petersen M, Broedbaek K, Andersen NL, Torp-Pedersen C, et al. Prevalence of antidepressant use during pregnancy in Denmark, a nation-wide cohort study. PLoS ONE. (2013) 8:e63034.
- Margulis AV, Kang EM, Hammad TA. Patterns of prescription of antidepressants and antipsychotics across and within pregnancies in a population-based UK ohort. Matern Child Health J. (2014) 8:1742–52.
- Munk-Olsen T, Gasse C, Laursen TM. Prevalence of antidepressant use and contacts with psychiatrists and psychologists in pregnant and postpartum women. Acta Psychiatr Scand. (2012) 125:318–24.
- Freeman MP. Antidepressant medication treatment during pregnancy: prevalence of use, clinical implications, and alternatives. J Clin Psychiatr. (2011) 72:977–8.
- Andrade SE, Raebel MA, Brown J, Lane K, Livingston J, Boudreau D, et al. Use of antidepressant medications during pregnancy: a multisite study. Am J Obstet Gynecol. (2008) 198:194. e1–5.
- Olfson M, Marcus SC. National patterns in antidepressant medication treatment. Arch Gen Psych. (2009) 66:848–56.
- Dunkel Schetter C. Psychological science on pregnancy: stress processes, biopsychosocial models, and emerging research issues. Ann Rev Psychol. (2011) 62:531–58.
- Martin RP, Dombrowski, Stefan C. Prenatal Exposures: Psychological and Educational Consequences for Children. New York, NY: Springer (2008).
- Rice F, Jones I, Thapar A. The impact of gestational stress and prenatal growth on emotional problems in offspring: a review. Acta Psychiatr Scand. (2007) 3:171–83.
- Blumberg SJ, Bramlett MD, Kogan MD, Schieve LA, Jones JR, Lu MC. Changes in prevalence of parent-reported autism spectrum disorder in school-aged US children: 2007 to 2011-2012. Natl Health Stat Rep. (2013) 20:1–11.
- Fombonne E. Epidemiology of pervasive developmental disorders. Pediatr Res. (2009) 65:591–8.
- Bailey A, Le Couteur A, Gottesman I, Bolton P, Simonoff E, Yuzda E, et al. Autism as a strongly genetic disorder: evidence from a British twin study. Psychol Med. (1995) 25:63–77.
- Smalley SL, Asarnow RF, Spence MA. Autism and genetics: a decade of research. Arch Gen Psychiatr. (1988) 45:953–61.
- Bristol MM, Cohen DJ, Costello EJ, Denckla M, Eckberg TJ, Kallen R, et al. State of the science in autism: report to the national institutes health. J Autism Dev Disord. (1996) 26:121–54.
- Trowbridge S, Narboux-Neme N, Gaspar P. Genetic models of serotonin (5-HT) depletion: what do they tell us about the developmental role of 5-HT? Anatomical Record. (2011) 294:1615–23.
- Narboux-Neme N, Pavone LM, Avallone L, Zhuang X, Gaspar P. Serotonin transporter transgenic (SERTcre) mouse line reveals developmental targets of serotonin specific reuptake inhibitors (SSRIs). Neuropharmacology. (2008) 55:994–1005.
- Gaspar P, Cases O, Maroteaux L. The developmental role of serotonin: news from mouse molecular genetics. Nat Rev Neurosci. (2003) 4:1002–12.
- Vitalis T, Cases O, Passemard S, Callebert J, Parnavelas JG. Embryonic depletion of serotonin affects cortical development. Eur J Neurosci. (2007) 26:331–44.
- Vitalis T, Parnavelas JG. The role of serotonin in early cortical development. Develop Neurosci. (2003) 25:245–56.
- Cases O, Vitalis T, Seif I, De Maeyer E, Sotelo C, Gaspar P. Lack of barrels in the somatosensory cortex of monoamine oxidase A-deficient mice: role of a serotonin excess during the critical period. Neuron. (1996) 16:297–307.
- El Marroun H, Jaddoe VW, Hudziak JJ, Roza SJ, Steegers EA, Hofman A, et al. Maternal use of selective serotonin reuptake inhibitors, fetal growth, and risk of adverse birth outcomes. Arch Gen Psychiatr. (2012) 69:706–14.
- Chambers CD, Johnson KA, Dick LM, Felix RJ, Jones KL. Birth outcomes in pregnant women taking fluoxetine. N Eng J Med. (1996) 335:1010–5.
- Alwan S, Reefhuis J, Rasmussen SA, Olney RS, Friedman JM, National Birth Defects Prevention S. Use of selective serotonin-reuptake inhibitors in pregnancy and the risk of birth defects. N Eng J Med. (2007) 356:2684–92.
- Malm H, Artama M, Gissler M, Ritvanen A. Selective serotonin reuptake inhibitors and risk for major congenital anomalies. Obst Gynecol. (2011) 118:111–20.
- Berard A, Zhao JP, Sheehy O. Antidepressant use during pregnancy and the risk of major congenital malformations in a cohort of depressed pregnant women: an updated analysis of the Quebec Pregnancy Cohort. BMJ Open. (2017) 7:e013372.
- Berard A, Zhao JP, Sheehy O. Sertraline use during pregnancy and the risk of major malformations. Am J Obstet Gynecol. (2015) 212:795e1–12.
- Berard A, Sheehy O, Zhao JP, Vinet E, Bernatsky S, Abrahamowicz M. SSRI and SNRI use during pregnancy and the risk of persistent pulmonary hypertension of the newborn. Br J Clin Pharmacol. (2017) 83:1126–33.
- Kieler H, Artama M, Engeland A, Ericsson O, Furu K, Gissler M, et al. Selective serotonin reuptake inhibitors during pregnancy and risk of persistent pulmonary hypertension in the newborn: population based cohort study from the five Nordic countries. BMJ. (2012) 344:d8012.
- Jensen HM, Gron R, Lidegaard O, Pedersen LH, Andersen PK, Kessing LV. Maternal depression, antidepressant use in pregnancy and Apgar scores in infants. Br J Psychiatr. (2013) 202:347–51.
- Andalib S, Emamhadi MR, Yousefzadeh-Chabok S, Shakouri SK, Høilund- Carlsen PF, et al. Maternal SSRI exposure increases the risk of autistic offspring: a meta-analysis and systematic review. Eur Psychiatr. (2017) 45:161–6.
- Boukhris T, Sheehy O, Mottron L, Bérard A. Antidepressant use during pregnancy and the risk of autism spectrum disorder in children. JAMA Pediatr. (2016) 170:117–24. doi: 10.1001/jamapediatrics.2015.3356
- Croen LA, Grether JK, Yoshida, CK, Odouli R, Hendrick V. Antidepressant use during pregnancy and childhood autism spectrum disorders. Arch Gen Psychiatr. (2011) 68:1104–12.
- El Marroun TJ, White NJ, Homberg G, Schoemaker NK, Jaddoe VW, Hofman A, et al. Prenatal exposure to selective serotonin reuptake inhibitors and social responsiveness symptoms of autism: population-based study of young children. Br J Psychiatr. (2014) 205:95–102.
- Gidaya NB, Lee BK, Burstyn I, Yudell M, Mortensen EL, Newschaffer CJ. In utero exposure to selective serotonin reuptake inhibitors and risk for autism spectrum disorder. J Autism Develop Dis. (2014) 44:2558–67.
- Hagberg KW, Robijn AL, Jick S. Maternal depression and antidepressant use during pregnancy and the risk of autism spectrum disorder in offspring. Clin Epidemiol. (2018) 10:1599–612.
- Kaplan YC, Keskin-Arslan E, Acar S, Sozmen K. Maternal SSRI discontinuation, use, psychiatric disorder and the risk of autism in children: a meta-analysis of cohort studies. Br J Clin Pharmacol. (2017) 83:2798–806.
- Kobayashi T, Matsuyama T, Takeuchi M, Ito S. Autism spectrum disorder and prenatal exposure to selective serotonin reuptake inhibitors: A systematic review and meta-analysis. Reproduct Toxicol. (2016) 65:170–8.
- Halvorsen A, Hesel B, Østergaard SD, Danielsen AA. In utero exposure to selective serotonin reuptake inhibitors and development of mental disorders: a systematic review and meta-analysis. Acta Psychiatr Scand. (2019) 139:493– 507.
- Harrington RA, Lee LC, Crum RM, Zimmerman AW, Hertz- Picciotto I. Prenatal SSRI use and offspring with autism spectrum disorder or developmental delay. Pediatrics. (2014) 133:e1241–8.
- Hviid A, Melbye M, Pasternak B. Use of selective serotonin reuptake inhibitors during pregnancy and risk of autism. N Eng J Med. (2013) 359:2406–15.
- Kim JY, Son MJ, Son CY, Radua J, Eisenhut M, Gressier F, et al. Environmental risk factors and biomarkers for autism spectrum disorder: an umbrella review of the evidence. Lancet Psychiatr. (2019) 6:590–600.
- Malm H, Brown AS, Gissler M, Gyllenberg D, Hinkka-Yli-Salomäki S, McKeague IW, et al. Gestational exposure to selective serotonin reuptake inhibitors and offspring psychiatric disorders: a national register-based study. J Am Acad Child Adolesc. (2016) 55:359–66.
- Man KK, Tong HH, Wong LY, Chan EW, Simonoff E, Wong IC. Exposure to selective serotonin reuptake inhibitors during pregnancy and risk of autism spectrum disorder in children: a systematic review and meta- analysis of observational studies. Neurosci Biobehav Rev. (2015) 49:82–9.
- Morales D, Slattery J, Evans S, Kurz X. Antidepressant use during pregnancy and risk of autism spectrum disorder and attention deficit hyperactivity disorder: systematic review of observational studies and methodological considerations. BMC Med. (2018) 16:6.
- Rai D, Lee BK, Dalman C, Golding J, Lewis G, Magnusson C. Parental depression, maternal antidepressant use during pregnancy, and risk of autism spectrum disorders: population based case-control study. BMJ. (2013) 346:f2059.
- Rai D, Lee BK, Dalman C, Newschaffer C, Lewis G, Magnusson C. Antidepressants during pregnancy and autism in offspring: population based cohort study. BMJ. (2017) 358:j2811. doi: 10.1136/bmj.j2811
- Sørensen MJ, Grønborg TK, Christensen J, Parner ET, Vestergaard M, Schendel D, et al. Antidepressant exposure in pregnancy and risk of autism spectrum disorders. Clin Epidemiol. (2013) 5:449–59
- Zhou XH, Li YJ, Ou JJ, Li YM. Association between maternal antidepressant use during pregnancy and autism spectrum disorder: an updated meta- analysis. Mol Autism. (2018) 9:21.
- Glover ME, Clinton SM. Of rodents and humans: A comparative review of the neurobehavioral effects of early life SSRI exposure in preclinical and clinical research. Int J Dev Neurosci. (2016) 51:50–72.
- Maciag D, Simpson KL, Coppinger D, Lu Y, Wang Y, Lin RC, et al. Neonatal antidepressant exposure has lasting effects on behavior and serotonin circuitry. Neuropsychopharma. (2006) 31:47.
- Glover ME, Pugh PC, Jackson NL, Cohen JL, Fant AD, Akil H, et al. Early-life exposure to the SSRI paroxetine exacerbates depression-like behavior in anxiety/depression-prone rats. Neuroscience. (2015) 284:775–97.
- Sprowles JL, Hufgard JR, Gutierrez A, Bailey RA, Jablonski SA, Williams MT, et al. Perinatal exposure to the selective serotonin reuptake inhibitor citalopram alters spatial learning and memory, anxiety, depression, and startle in Sprague-Dawley rats. Int J Develop Neurosci. (2016) 54:39–52.
- Vorhees CV, Acuff-Smith KD, Schilling MA, Fisher JE, Moran MS, Buelke-Sam J. A developmental neurotoxicity evaluation of the effects of prenatal exposure to fluoxetine in rats. Toxicolog Sci. (1994) 23:194–205.
- Evans J, Heron J, Francomb H, Oke S, Golding J. Cohort study of depressed mood during pregnancy and after childbirth. BMJ. (2001) 323:257–60.
- Jimenez-Solem E, Andersen JT, Petersen P, Broedbaek K, Jensen JK, Afzal S, et al. Exposure to selective serotonin reuptake inhibitors and the risk of congenital malformations: A nationwide cohort study. BMJ Open. (2012) 2:1–9.
- Josefsson A, Berg G, Nordin C, Sydsjo G. Prevalence of depressive symptoms in late pregnancy and postpartum. Acta Obst Gynecol Scand. (2001) 80:251–5. doi: 10.1034/j.1600-0412.2001.080003251.x
- Lund N, Pedersen LH, Henriksen TB. Selective serotonin reuptake inhibitor exposure in utero and pregnancy outcomes. Arch Pediatr Adolescent Med. (2009) 163:949–54.
- Olesen C, Thrane N, Nielsen GL, Sorensen HT, Olsen J. A population-based prescription study of asthma drugs during pregnancy: Changing the intensity of asthma therapy and perinatal outcomes. Respiration. (2001) 68:256–61.
- Susser E, Eide MG, Begg M. Invited commentary: The use of sibship studies to detect familial confounding. Am J Epidemiol. (2010) 172:537–9.
- Frisell T, Oberg S, Kuja-Halkola R, Sjolander, A. Sibling comparison designs: bias from non-shared confounders and measurement error. Epidemiology. (2012) 23:713–20. doi: 10.1097/EDE.0b013e31825fa230
- Viktorin A, Levine SZ, Altemus M, Reichenberg A., Sandin S. Paternal use of antidepressants and offspring outcomes in Sweden: nationwide prospective cohort study. BMJ. (2018) 361:k2233.
- Anderson GM, Czarkowski K, Ravski N, Epperson CN. Platelet serotonin in newborns and infants: ontogeny, heritability, and effect of in utero exposure to selective serotonin reuptake inhibitors. Pediatric Res. (2004) 56:418.
- Cook EH, Leventhal BL, Freedman DX. Free serotonin in plasma: autistic children and their first-degree relatives. Biol Psychiat. (1988) 24:488–91.
- Fatima Z, Zahra A, Ghouse M, Wang X, Yuan Z. Maternal SSRIs experience and risk of ASD in offspring: a review. Toxicol Res. (2018) 7:1020–8.
- Reefhuis J, Devine O, Friedman JM, Louik C, Honein MA. Specific SSRIs and birth defects: Bayesian analysis to interpret new data in the context of previous reports. BMJ. (2015) 351:h3190.
- Petersen I, McCrea RL, Lupattelli A, Nordeng H. Women’s perception of risks of adverse fetal pregnancy outcomes: a large-scale multinational survey. BMJ Open. (2015) 5:e007390.
- Sujan AC, Oberg S, Quinn PD, D’Onofrio BM. Annual research review: maternal antidepressant use during pregnancy and offspring neurodevelopmental problems – a critical review and recommendation for future research. J Child Psychol Psychiatr. (2019) 60:356–76.



